英国《泰晤士报》3月16日报道中说:“全球争相研发新冠肺炎疫苗的行为如同抽彩票,获胜与否并不是那么取决于研发的速度甚至是技术,运气似乎也很重要。”
这场疫苗竞赛,运气固然重要,但事实上,硬核科研实力才是入场券。
这场竞赛,也为我们展示了mRNA和DNA等新型疫苗的未来。
—mRNA和DNA等新型疫苗的未来
尽管很多人认为,“远水救不了近火“,等到疫苗可用的时候,疫情或许已经过去。但目前全球包括中国、美国、英国、法国、澳大利亚等国家的研究人员仍在积极投入新型冠状病毒疫苗的研制。一场与病毒“抢时间”的疫苗竞赛也随之展开。
据澎湃新闻数据统计,全球共计40余家研发团队正在进行新冠疫苗的研发。进展较快的目前有中国李兰娟院士的重组疫苗,和美国Moderna的mRNA疫苗。另外还有4家研发团队也预计将很快进入临床试验,分别是:艾棣维欣+inovio;中国疾控中心+上海同济医学院+斯微生物;英国帝国理工;BioNTech+复星
军事科学院军事医学研究院陈薇院士领衔研制的重组新冠疫苗已获批启动展开临床试验:
军事科学院军事医学研究院陈薇院士团队联合武汉地方优势企业,在埃博拉疫苗成功研发的经验基础上,争分夺秒开展重组新型冠状病毒疫苗的药学、药效学、药理毒理等研究,快速完成了新冠疫苗设计、重组毒种构建和GMP条件下生产制备,以及第三方疫苗安全性、有效性评价和质量复核。3月16日晚,其重组新冠疫苗通过了临床研究注册审评,获批进入临床试验。而且该疫苗已经做好了安全、有效、质量可控、可大规模生产的前期准备工作。
西雅图第一批志愿者开始接种美国生物科技公司Moderna研制的新冠肺炎候选疫苗:
3月16日,第一批临床试验志愿者在美国西雅图接受注射。该疫苗项目的发起者是美国国立卫生研究院(NIH)和美国生物科技公司Moderna,前者同时是项目资助方。Moderna此次疫苗为mRNA疫苗。
中德合作研发新冠疫苗:
总部位于德国美因茨的生物技术公司BioNTech公司16日发布声明,从复星医药获得高达1.2亿欧元的投资,合作研制基于mRNA技术的新冠疫苗,并将于4月底开始首次临床试验。
疾控中心+同济大学+斯微生物:
距离中国疾控中心1月24日成功分离我国首株新型冠状病毒毒种仅两周时间,中国疾控中心、上海同济大学医学院和上海生物技术公司斯微生物,在2月宣布最新研发的新型冠状病毒疫苗已开始动物试验。
艾棣维欣+inovio:
Inovio与北京艾棣维欣生物技术有限公司(BeijingAdvaccineBiotechnologyCo)携手加快在中国开发INO-4800。已经开始临床前测试和准备,以便为临床产品生产做准备。此次合作旨在利用艾棣维欣的技术在中国进行一期试验,配合Inovio在美国的临床开发工作。Inovio参与这项开发工作是基于其DNA药物平台快速开发针对新型流行病毒的疫苗的能力、久经考验的疫苗开发能力,以及快速生成应对先前流行病威胁的有效对策的丰富经验。
mRNAvsDNA,谁会更快?
传统的疫苗开发是一个漫长的过程。传统疫苗是把减毒或者灭活后的病原体,或者病原体的一部分(抗原)注射进人体,人的免疫系统识别抗原后,通过免疫反应产生抗体。传统疫苗研发风险比较低,但筛选减毒/纯化的病原体株时间较长,同时疫苗生产工艺繁杂,不适合突发疫情的快速响应。
受益于新技术的发展,疫苗开发周期从过去的几年缩短至几个月。其中的主力军便是mRNA和DNA疫苗。
颠覆性的mRNA平台
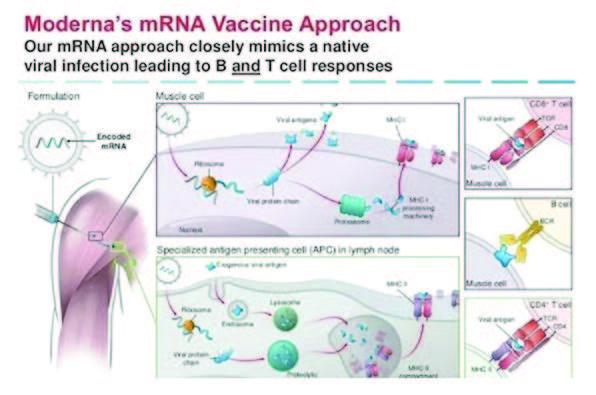
mRNA是一种新的疫苗技术,注射进人体的不是病原体本身,而是特异的病原体mRNA序列,脂质体包裹的mRNA注射后进入肌肉细胞,被转录成病原体特异的蛋白,并表达在MHC1受体上,DentriticCell可以识别肌肉细胞上表达的病原体蛋白,激发免疫反应产生抗体。
简单来说,mRNA疫苗模拟了自然病毒感染发生的过程,诱导人体细胞产生与病原体表面相同的蛋白,激活免疫反应,犹如在人体内建造一座“制药厂”。
与灭活疫苗不同,mRNA疫苗不具有与感染相关的风险,可以提高接种安全性。最重要的是,免去了繁杂的菌株筛选过程,只要涉及mRNA序列,合成,脂质体包裹,简单几步就能少量生产,把时间留给后面的临床。
但它进入临床试验还需要必经的步骤,根据试验周期和病人的情况,临床试验周期可能从几个月至几年不等。且面临工业制造流程不成熟、价格昂贵的问题。
这次美国的Moderna就是mRNA疫苗:
国内,中国疾控中心、上海同济大学医学院和上海生物技术公司斯微生物共同设计开发的mRNA疫苗被认为是对标Moderna的产品。
根据斯微生物方面透露,1月底研发人员在获得中国疾控中心提供的新型冠状病毒抗原后,就开始了两周的疫苗研制工作。该疫苗是基于mRNA(信使核糖核酸)平台开发的,mRNA是DNA单链转录而来,和DNA一样也携带遗传信息,能够指导蛋白合成。此外,在疫苗的动物试验中使用了9至12种不同的抗原。
同济大学附属东方医院院长刘中民教授:“基于mRNA的疫苗开发是至今为止最有效和最先进的方法之一,大大地缩短了疫苗的研发周期。”
“与传统疫苗相比,mRNA疫苗技术在疗效、研发速度、生产的可拓展性和安全性等方面具有巨大优势。多种病毒抗原能够整合进一条mRNA,从而可以生产传统技术难以实现的复杂多抗原疫苗。”
业内普遍认为mRNA药物平台将有望成为颠覆性迭代产品。目前,全球范围内治疗性疫苗的头部企业都将mRNA疫苗作为重要的研发方向,如Moderna、CureVac、BioNTech等。
DNA新型基因工程疫苗
除了mRNA的方法,基于DNA也能够快速开发出疫苗。美国生物企业Inovio就在中国科学家将新冠病毒的基因组序列发布到公共数据库的第二天,启动了新冠病毒的研发计划。他们针对新冠病毒的刺突蛋白设计DNA疫苗,并在两天之内就设计出一种针对刺突蛋白的疫苗。
InovioCEOJosephKim表示,公司根据病毒的基因序列开发疫苗,比使用病毒实体进行试验的传统实验室做法,效率更高速度更快。1月28日,Inovio与位于苏州的生物医药企业艾棣维欣生物展开合作,采用最新DNA疫苗技术,共同开发疫苗,并称争取在最短时间内将疫苗在中国推进至临床试验阶段。
Inovio有长期的DNA药物平台快速开发针对新型流行病毒的疫苗的开发经验,是首家将针对相关冠状病毒MERS-CoV的疫苗(INO-4700)用于人体试验的公司之一。Inovio目前准备在中东地区启动INO-4700的二期疫苗试验,大多数MERS病毒爆发都发生在中东。
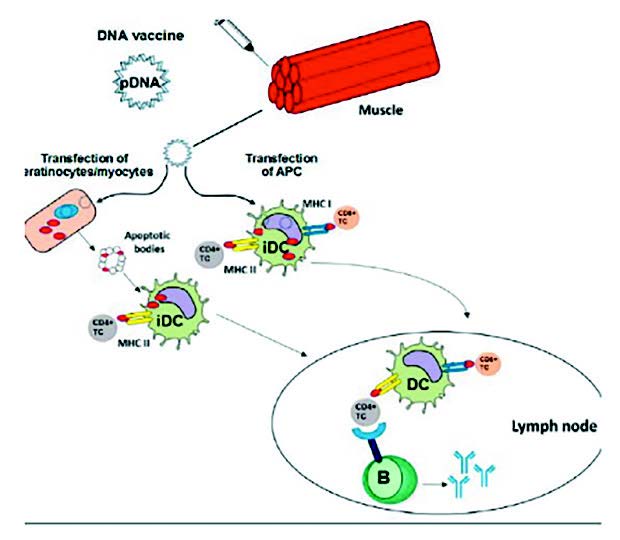
DNA疫苗需要先编码目的抗原蛋白基因序列的质粒,然后经肌肉注射导入宿主细胞,通过转录系统表达抗原蛋白,诱导宿主产生针对该抗原蛋白的免疫应答,从而达到免疫目的,属于一种新型基因工程疫苗。
与传统的诱导抗原特异性免疫反应的蛋白/肽的疫苗相比,DNA疫苗会更稳定,更经济,更容易生产和更安全。DNA疫苗正被研究用于各种各样的应用,包括癌症的治疗、过敏、自身免疫疾病和传染病。在美国,已有超过500个以DNA接种疫苗为重点的临床试验注册。
DNA疫苗也面临着很多未知风险,比如基因表达失调和突变的可能性,以及免疫反应是否足以产生显著的临床效益,等等。
远水救不了近火?
急性传染病疫情的爆发终究是不稳定的。如开头所说,一旦结束,没有患者可供临床试验,政府和药企也失去了动力继续投资。
但如果新冠肺炎演变为慢性病或季节性流行病,或者冠状病毒在未来再次引发新型疾病,研发疫苗的价值就会显现。
“我们不能指望(新冠肺炎)会像流感一样会消失在夏天”,世卫组织突发卫生事件规划执行主任MikeRyan在3月6日的一场发布会上提到。“所以我们得斗争,而不是干等着病毒自己消失。”
疫苗和免疫规划专家陶黎纳在接受媒体采访时也表示,2003年暴发的SARS、2012年暴发的MERS,加上今年的新冠肺炎,“21世纪以来,就已经出现了3种大规模感染人类的冠状病毒。三连击之后,我们才意识到将来说不定还有第四种,才下定决心研发针对冠状病毒的疫苗。”
以埃博拉病毒为例,2014年病毒首次在西非暴发时,没有疫苗可用,然而在2019年刚果再次暴发埃博拉疫情时,有超过20万人注射了埃博拉疫苗,及时地抑制了疫情的扩散。
疫苗的资本支持是个问题,但还是架不住各个药企希望就此拔得头筹。据新华网记载,非典期间,如果成熟的药品拿到新药证书,会有几千万甚至是上亿的转让费;当疫苗成果转化为企业产品后,市场价值还将扩大100倍。
不过,抛开资本和商机,我们依然开心地看到,在这次的疫情中,全世界对基础科研难得默契地、展现出了空前的支持!
作者:姚舜Daisy