荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
绝大部分传统植物提取流程在植物收获和干燥之后才可进行。生长、收获和干燥条件中的可变因素会严重影响植物原料成分的再现性。即便是连续变化较少的单一因素,在共同作用的情况下也会显著降低植物原料成分和特性的再现性。假设生长、收获和干燥阶段的再现率为80%,那么干燥植物原料的变化率约为50%(0.8×0.8=~0.5)。此外,干燥过程会产生不必要的渗压震扰和氧化应激反应,导致植物细胞去区室化,破坏植物酶,引发水解作用、酚类聚合反应、美拉德反应、异构化反应,促使糖苷转化为糖苷配基,造成微生物污染。传统提取技术仅能提取分解代谢过程的“幸存者”,即干燥植物中的分解代谢物和相对稳定的化合物。这些条件会对众多最终提取物的再现性、功效、生物利用度及安全性产生不利影响。而这些提取物的成分仅对特定的溶剂具有亲和力,所以其应用受限。传统提取技术无法提取活体植物细胞中的所有活性物质,而且会破坏不同化合物之间的自然协同作用,进而削弱或彻底丧失所需的天然化合物多功能特性。例如,传统提取技术无法获取活性伏牛花中黄连素和5’-甲氧基次大风子素的协萃络合物[2]。重要的是,传统植物提取技术通常会使用离子交换树脂和大量有机溶剂(每提取1 千克提取物有时需要10升溶剂),这就需要消耗大量能量,而溶剂蒸发和再生会进一步增加能耗。而超临界CO2萃取技术只不过是己烷萃取的替代技术,无法广泛应用。为了解决这一问题,“Zeta Fraction”可持续性无溶剂提取技术(ZFT)应运而生[4-8]。
“Zeta Fraction”技术(ZFT)的原理
活体植物由于具有较高代谢活性,因此是获取所有天然复合物及化合物的最佳来源。活性细胞的内部动态平衡可将植物原料的主要物理化学特性值维持在相对较小的浮动范围内,优于任何干燥和储存方法。鉴于植物活力取决于光合活性水平,ZFT 把对光合活性水平(以及许多其他参数)的验证作为重要的质量控制因素。测定光系统Ⅱ的叶绿素荧光参数值[9] 能够有效区分活体植物和非活体植物,而ZFT 仅选择活体植物进行后续处理。为避免破坏天然有益复合物及化合物的完整性,理想的初始原料应选取缺少厚壁机械组织的活体植物。原生质体的大规模工业级培养目前尚不可行,而且无法复制供植物合成所有天然复合物及化合物(包括次生代谢产物)所需的代谢环境。因此,实用的做法是通过机械法实现细胞内胶态分散体和细胞壁的迅速分离。
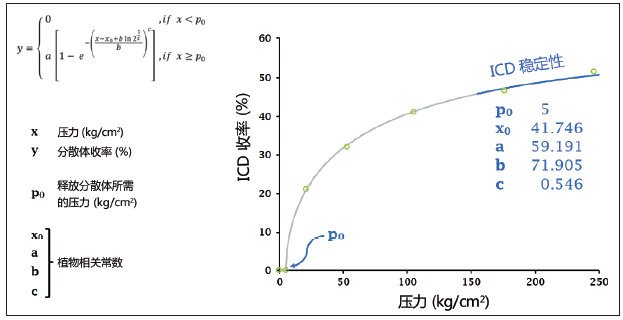
图1. 活性鼠尾草细胞内胶态分散体的收率曲线参数
为了获取与原始细胞内含物完全匹配且相对稳定的细胞内胶态分散体(ICD),必须使用外源酶,因为机械力无法让所有类型的活体植物细胞内含物(如细胞器、天然复合物及化合物)以相同的速度移动或缓慢移动。通过趋近收率曲线的稳定性(S)临界区域(如图1 所示),渐近近似法可在不使用外部化学物质(如酶)的情况下获取ICD。图1展示了活性鼠尾草的收率曲线参数。对于不同植物而言,实现原始细胞内含物和稳定性水平之间高度匹配所需的相关参数和条件不尽相同。这些实验数据与威布尔分布模型[10]最为匹配。
ZFT 专用移动车辆可立即处理分离后获取的相对稳定的ICD,每次可处理约10吨活体植物。遵循“技术应用于植物”(而非“植物应用于技术”)的原则,这项策略可防止出现不必要的分解代谢过程,改善对天然复合物及化合物的保护,同时提高再现水平。对部分植物(14个植物科中的代表性物种)ICD的物理化学测试表明,各个因素的变化率有高有低(如固体含量、传导率和pH 值的变化率分别为~80%、~50% 和~40%,而同渗容摩和介电常数的变化率仅为~5%)。因此,植物的同渗容摩[11]和介电常数[12]可作为关键参数用于所有植物且彼此保持一致。图2 表明介电常数(实部)的变化率显著较低,展示了从14 个植物科中选出的部分植物的ICD均值和95%置信区间。
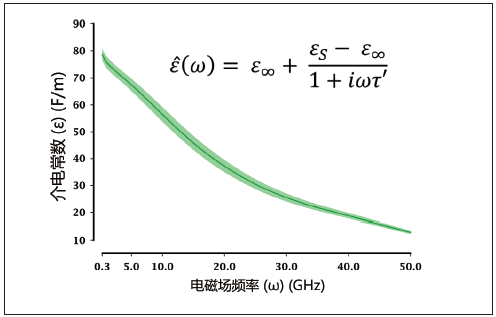
图2:从14个植物科中选出的部分植物ICD的德拜方程和介电常数(实部)
从ZFT的角度而言,所获取的细胞内物质为相对稳定的胶态分散体,且含有连续相(细胞质和液泡内含物)和分散相(悬浮细胞器及其碎片)。依据Derjaguin-Laundau-Verwey-Overbeek(DLVO)理论,分散体稳定性取决于范德瓦尔斯引力和双电层斥力的总和[13]。斥力所导致的能障会阻止分散相颗粒互相接近,除非它们具有足以克服能障的能量,此时它们会在引力的作用下互相接触(不可逆的粘附过程)。DLVO理论基于分散相颗粒的参数、彼此之间的距离和连续相的特性,对分散相颗粒之间的相互作用和势能进行了阐述。对变量值进行调整会改变斥力大小,进而影响分散体的稳定性(如图3 所示)。
图3以典型的叶绿体为例。图中的细点线代表双电层斥力(VD),细虚线代表范德瓦尔斯引力(VW),而粗实线代表前述两者和空间位阻斥力的总和。在正常条件下(红色),随着分散相颗粒互相接近,颗粒之间的势能会逐渐增加,进而形成势能障碍;在没有外部能量输入的情况下,颗粒无法克服该能障。颗粒在能障的作用下互相分离,此时分散体保持稳定。当条件改变时(青色),双电层斥力逐渐降低,直至势能障碍消失,此时颗粒可不受约束地互相接近和聚集。然而,回到初始条件后稳定性并不能恢复,因为颗粒聚集是不可逆过程,通过机械法可以轻松去除聚集的颗粒。如图2中的德拜方程[12] 所示,改变条件的方式之一是运用介电常数(ε)与电磁场频率(ω)之间的关系。
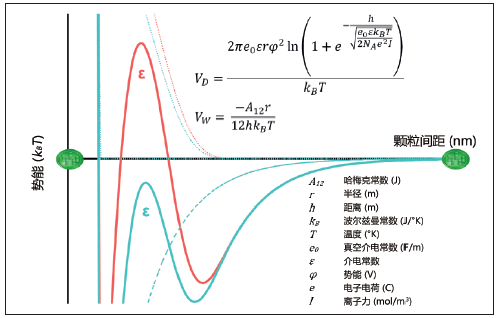
图3. 胶态分散体的稳定性和介电常数变动的影响
依据DLVO理论及Van’t-Hoff和Debye发现的基本科学原理,ZFT 对细胞内胶态分散体进行有针对性的去稳定化处理,然后经过分离形成不同的Zeta Fraction提取物。这一过程中的关键步骤包括:采集具有最高代谢活性的活体植物;分离细胞壁和相对稳定的ICD;对ICD进行处理,通过改变引力和斥力之间的平衡状态,让分散相和连续相中的特定组分产生特异性相互作用;以及分离ICD,形成不同的Zeta Fraction 提取物(如图4所示)。
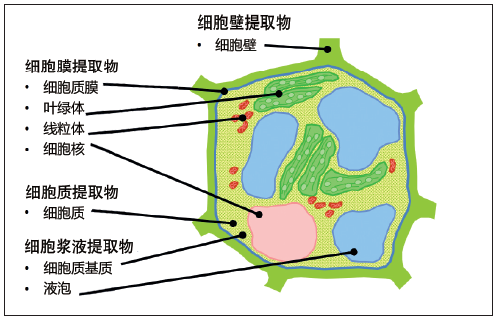
图4. Zeta Fraction 提取物所对应的活体植物细胞组分
研究发现,完成有针对性的ICD去稳定化处理仅需少量能量,远低于化学键能,因此可防止活体植物细胞组分的分子结构在ZFT处理过程中发生改变[8]。ZFT专用连续生产设备已完成设计和制造,目前正在探索如何提高其容量,以满足大规模生产Zeta Fraction提取物的需求。
可持续性
依据ISO 14040和ISO 14044标准,同时使用Ecoinvent数据库和PE International公司的GaBi生命周期评估软件包,从环境保护和可持续性的角度对ZFT 的完整过程进行了评估,以此展示这项无溶剂技术的优势。参考溶剂系统用于开展比较评估,系统内组分的介电常数介于2.0-80.0 F/m。图5对比了分别使用ZFT和传统溶剂提取技术从活体茶树中提取1000千克添加剂所产生的环境影响。如评估中考虑到有害溶剂给工人和环境带来的安全风险,ZFT的优越性会更加明显。
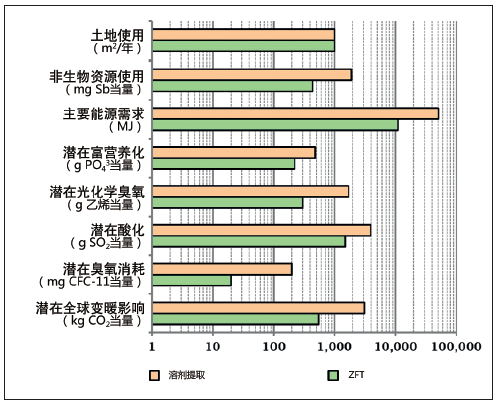
图5. 分别使用ZFT 和传统溶剂提取技术从活体茶树中提取添加剂所产生的环境影响对比
Zeta Fraction提取物的成分明显区别于通过传统溶剂技术获取的同类提取物,前者含有的所需化合物占比更高,而且分布方式也完全不同。例如,ZFT可从同一种茶树品种中同时获取细胞浆液提取物、细胞质提取物、以及传统泡制的绿茶和红茶。图6展示了与儿茶素有关的分析数据。
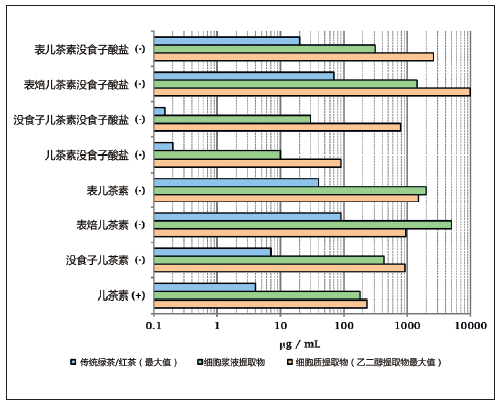
图6. Zeta Fraction 茶树提取物和传统泡制的绿茶/ 红茶成分对比
安全性和再现性
植物所含的多种天然复合物及化合物提供了众多强效特性和实现功能所需的协同效应,但也催生了颇具挑战的安全问题。实践证明,ZFT可成功去除提取自各种植物的生物功能添加剂中特定的不必要组分和有害化学物质。部分可去除的物质包括小白菊素[6](已知的皮肤致敏物,可引发接触性皮炎,见图7)、蛋白质和高分子量肽类(呼吸道致敏物)、展青霉素(具有皮肤毒性的霉菌毒素)、脱镁叶绿甲酯酸(光敏剂)、补骨脂素(光敏剂),以及重金属。此外,ZFT制取的所有研究用和商用添加剂的微生物成分全面优于工业标准。图7中的示例数据表明,在连续若干年内从来自不同种植者的茶树中提取的20批商用Zeta Fraction提取物(每批约500千克)均具有高度再现性。特别值得注意的是,这些提取物是在连续若干年内提取的,而且原料来自不同的种植者。季节更替会影响每英亩植物的Zeta Fraction提取物产量,但是丝毫不会改变由遗传基因预先确定的提取物成分。
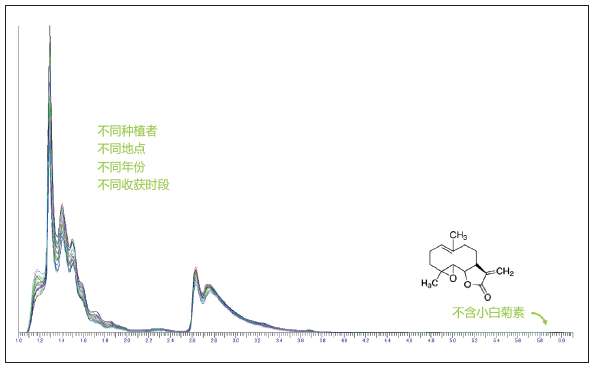
图7. Zeta Fraction 小白菊提取物不含任何有害化学物质(如小白菊素)
多功能特性
对添加剂而言,多功能特性是颇具吸引力的特性之一,因为健康而富有魅力的皮肤外观是多种复杂过程和路径共同作用的结果。皮肤刺激、炎症和色素沉着过度是常见的复杂皮肤问题,也是化妆品研发的重要课题。解决这些问题需要协调运用多种路径,而仅依靠单一化合物无法保证做到这一点。通过ZFT从活体莲中提取的特殊添加剂是最具代表性的例子之一,具有所需的多功能特性(见下表1)。
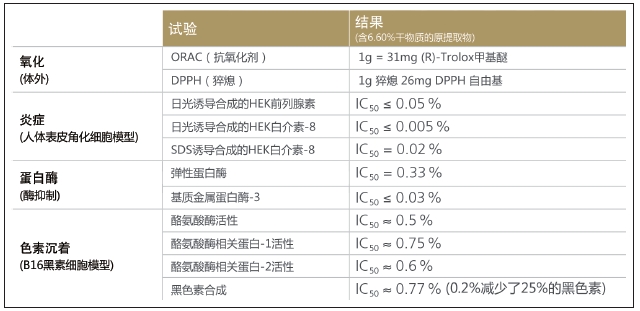
表1. Zeta Fraction 莲提取物的体外多功能特性
此外,位于法国索菲亚科技园的亚什兰全球皮肤研究中心对Zeta Fraction 莲提取物做了进一步分析。研究人员发现该添加剂具有如下功效:(1)提高透明质酸、丝聚合蛋白和水通道蛋白3(AQP3)的表达量,并降低黑色素在体外人体皮肤中的表达量;(2)提高胶原蛋白1 型在成人纤维母细胞中的表达量;(3)在对体外人体皮肤进行添加剂预处理的情况下,可改善皮肤弹性纤维的组织结构;(4)减少由十二烷基磺酸钠(SDS)引发的应激反应对3D 重建人体表皮屏障的破坏。临床研究表明,该添加剂还能(1)改善皮肤的保湿功能,减少表皮水分流失,同时让皮肤更加柔软(对比安慰剂);(2)改善皱纹外观(数量、深度、面积)和皮肤粗糙度;(3)改善皮肤外观,如皮肤引流和形体轮廓。
Zeta Fraction莲提取物的安全性和毒理学特征表明,其不会对皮肤和眼睛产生任何刺激(重建人体表皮试验、48小时人体皮肤斑贴试验、鸡胚绒毛膜尿囊膜试验、重建人体角膜上皮试验,浓度100%),而且不具有致敏性(人体皮肤重复刺激斑贴试验,浓度10%,受试样本> 200)、光毒性(3T3 中性红摄取光毒性试验)和遗传毒性(Ames 细菌回复突变试验)。
结论
ZFT专有技术能够从活体植物中提取天然的多功能复合物及化合物。这项技术无需利用外部溶剂,即可完成对细胞组分的分离,最大限度地降低了能耗。ZFT 对环境的负面影响和产生的废物也处于最低水平。ZFT实现了对供应链(从植物培育到提取物生产)的完整控制, 同时也为Zeta Fraction提取物的知识产权保护提供了全新的支持方式。Zeta Fraction提取物具有卓越的功效、安全性和再现性,而且单一添加剂可作用于多种路径。ZFT能够充分挖掘活体植物的应用潜力,并与现有的提取技术结合使用,实现有效减容。
参考文献
1. Feller, W. An introduction to probability theory and its applications: volume I.Vol. 3.London-New York-Sydney-Toronto: John Wiley & Sons, 1968.
2. Stermitz, F. R., Lorenz, P., Tawara, J. N., Zenewicz, L. A., & Lewis,K. (2000).Synergy in a medicinal plant: antimicrobial action of berberine potentiated by 5'-methoxyhydnocarpin, a multidrug pump inhibitor.
Proceedings of the National Academy of Sciences, 97(4), 1433-1437.
3. Callaghan, T., Oddos, T., Gendimenico, G., Martin, K. Method for the topical treatment and prevention of infkammatory disorders and relaterd conditiona using extracts of feverfew (Tanacetum parthenioum ).
4. U.S. Patent No. 7,229,650.Issued Date: June 12, 2007.
5. Koganov, M., U.S. Patent No. 7,442,391, Bioactive botanical cosmetic compositions and processes for their production.Issued Date: Oct. 28, 2008.
6. Koganov M., U.S. Patent 7,473,535, Bioactive compositions from Theacea plants and processes for their production and use.Issued Date: January 6, 2009.
7. Koganov, M., U.S. Patent No. 7,537,791, Parthenolide free bioactive ingredients from feverfew (Tanacetum parthenium ) and processes for their production.Issued Date: May 26, 2009.
8. Koganov, M., European Patent No. 1,722,805 B1, Bioactive compositions from theacea plants and processes for their production and use.Issued Date:Mar 26, 2014.
9. Koganov M., European Patent No. 2,919,757 B1, A method for preparing bioactive botanical compositions and the compositions made from said method using an electromagnetic field of greater than 3 GHz.Issued Date:October 5, 2016.
10. Maxwell K. and Johnson G.N., Chlorophyll fluorescence—a practical guide.Journal of Experimental Botany, (2000) 51 (345): 659-668.
11. Weibull, W., A statistical distribution function of wide applicability,Journal of Applied Mechanics., 1951, 18 (3): 293-297.
12. Van’t-Hoff, J. H., Osmotic pressure and chemical equilibrium, Nobel Lecture, Stockholm, Sweden, 1 (1901) 1-6.
13. Debye, P., Polar Molecules, Chemical Catalogue Company, New York,New York, USA, 1927, pp 143- 162.
14. Israelachvili, J.N., Intermolecular and Surface Forces, Academic Press,San Diego, California, USA, 1992, pp. 246-253.