荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
伴随着仿制药质量与疗效一致性评价工作政策的逐步清晰,国内制药企业如火如荼地推进该项工作,距离国家要求289个品种通过评价的时间节点2018年底,还有不到20个月的时间,而不在这289个品种中的其它已经备案的品种,目前是进展到什么情况等等,一系列问题还在不时困扰着企业。药包材药用辅料与药品关联审评审批制度已经2016年开始执行,但是制剂、医药包装、药用辅料企业执行过程中遇到一些需要协调的问题,也是需要有专家对常见具体问题进行解读。
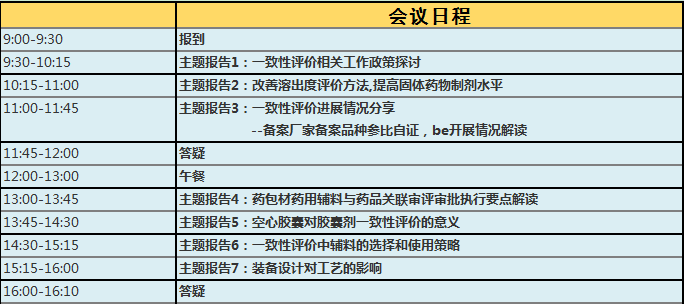
API China镇江巡回交流会计划邀请药品审评中心、中检院、药检所领导和专家,就仿制药质量和疗效一致性评价与关联审评审批热点问题进行解读,着眼评价过程和关联审评中遇到的实际问题,梳理思路,为一致性评价工作的顺利开展提供有意义的建议,携手行业栉风沐雨、砥砺前行。
会议听众免费
建议参会人群
l 知名制药企业的高级管理人员、总监、总工、研发主管、注册主管、研究人员、项目负责人。
l CRO公司、GCP、高校、科研院所、机构等单位的研发主管、项目负责人
l 医药包装企业和药用辅料企业的研发主管、注册主管
主办单位:国药励展
会议时间:2017年3月31日
会议地点:镇江碧榆园宾馆 会议中心一楼江州厅
会议地址:镇江市竹林路88号
报名联系人:刘 坤:010-84556542,13521635157,E-mail:kun.liu@reedsinopharm.com