荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
维也纳理工大学与庆应义塾大学的研究人员,发现了一种快速、可重复地在微型器官模型中创建人工血管的方法。该技术利用飞秒超短激光脉冲,在水凝胶中刻写出高度精细的三维结构。
在生物医学研究中,器官芯片正变得越来越重要:通过在精密控制的微流控芯片中培养组织结构,可以比使用活体人类或动物进行实验获得更准确的研究结果。
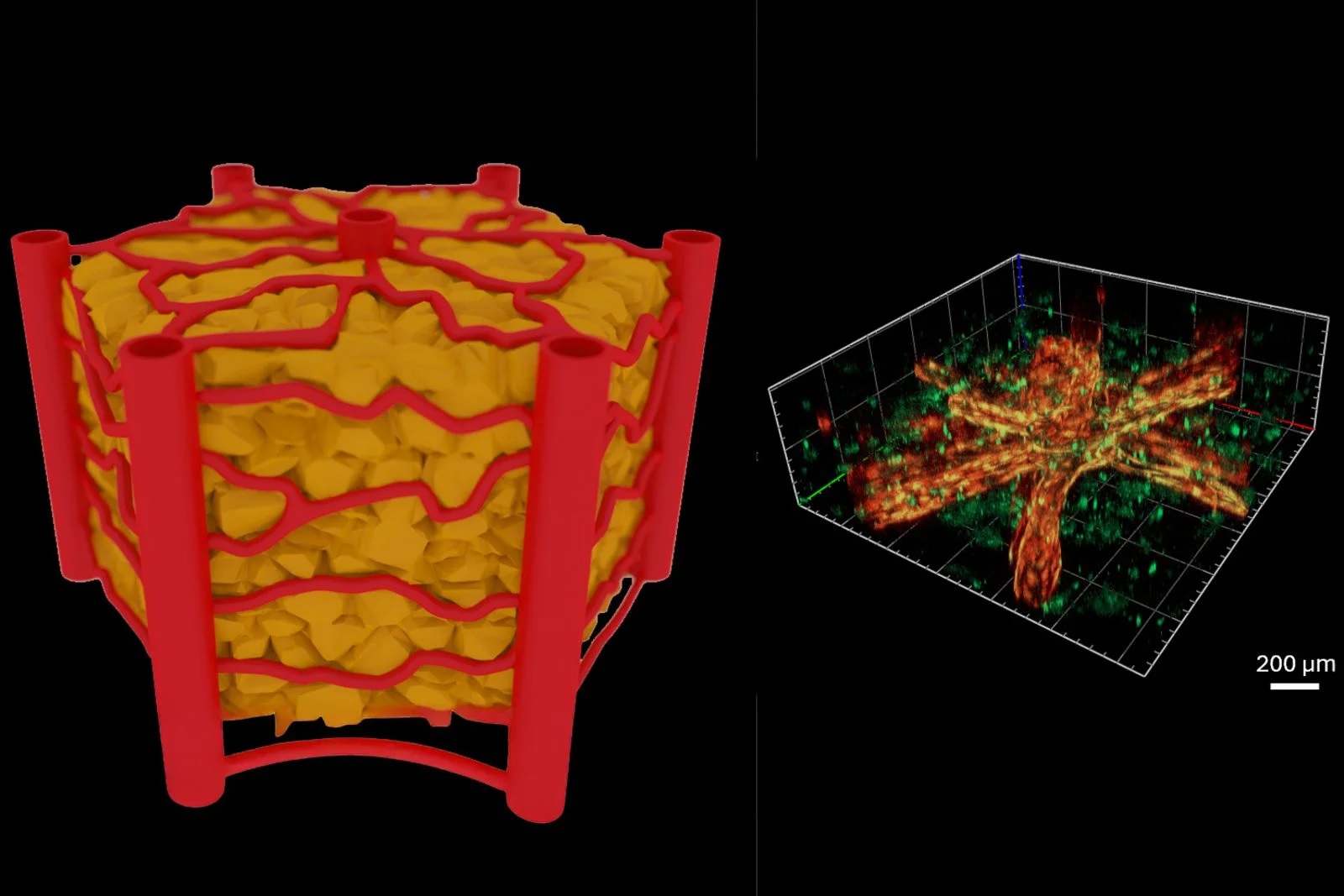
肝小叶结构示意图(左)与芯片上血管化肝小叶培养9天后的三维视图(右)
但始终存在一个主要障碍:这类微型器官若缺乏血管系统就不完整。为了促进系统性研究并确保与活体生物的有效对比,必须创建可灌注的血管和毛细血管网络——且构建方式必须精确可控、结果可重复。
“若要研究特定药物如何在不同人体组织中运输、代谢和吸收,就需要最精细的血管网络,”维也纳理工大学研究员Alice Salvadori解释道。目前这类微血管网络的形状和尺寸仍难以控制。基于自组织的方法中,不同样本间的血管几何结构差异显著,导致无法开展生物医学研究所需的、具备重复性的精密控制实验。
“我们能创建间隔仅百微米的通道。这在复制特定器官中血管自然密度时至关重要,”Aleksandr Ovsianikov表示。精度并非唯一要求:人工血管必须快速成型,并在植入活细胞后保持结构稳定。“我们知道细胞会主动重塑周围环境,这可能导致血管变形甚至塌陷,”Salvadori指出,“因此我们还优化了材料制备工艺。”
团队摒弃标准的一步凝胶法,采用两步热固化工艺:分两个温度阶段对水凝胶加热而非单一温度。这改变了其网络结构,生成更稳定的材料。其中形成的血管能长期保持通畅和形态稳定。
“我们不仅证明了可制造真正可灌注的人工血管,更重要的是开发出了适用于工业规模的可扩展技术,”Ovsianikov强调,“30条血管通道的图案化仅需10分钟,效率至少是其他技术的60倍。”
要在芯片上真实模拟生物过程,人工组织必须表现出与天然组织相同的特性。“我们证实这些人工血管能被内皮细胞成功定植,且其反应与体内真实血管完全一致,”Salvadori举例说,“例如对炎症的反应相同——通透性增加,就像真实血管那样。”
研究者认为,这标志着器官芯片技术向成为医学研究多领域工业标准迈出了重要一步。庆应义塾大学的Masafumi Watanabe表示:在器官芯片研究中,复制肝脏致密复杂的微血管系统长期存在挑战。通过构建贯穿整个组织体积的多层微血管,我们确保了充足的营养和氧气供应——进而提升了肝脏模型的代谢活性。相信这些进展让我们更接近将器官芯片技术整合到临床前药物研发的阶段。

