荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
细胞老化并非一夜之间降临,它悄然潜行,在染色体最末端的“生命刻度”——端粒上,留下肉眼看不见的痕迹。端粒,每细胞分裂一次便缩短一分,直至触碰“寿命底线”。而如何减缓这一缩短过程,始终是生命科学与抗衰老医学关注的核心。
近日,美国最大型学术医疗系统之一——麻总百瀚(Mass General Brigham, MGB)联合佐治亚医学院,基于 VITAL 随机对照研究发布最新发现——每日补充 2000 IU 的维生素 D3,可显著减缓白细胞端粒长度(LTL)的缩短速度,某种程度上相当于“抵消”了近三年自然老化进程。
去年《happi China》2024 年7月刊中,我们曾在《新型维生素 D 衍生物的皮肤抗老化潜力》这篇文章中梳理维生素 D 在护肤领域的前沿研究。如今,新试验又揭示维生素 D3 在人体层面减缓端粒缩短的新证据,今天这篇文章将带领读者进一步审视这颗“阳光维生素”在抗衰干预中的潜在版图。

此次研究的牵头机构麻总百瀚(Mass General Brigham, MGB),前身为 Partners HealthCare,是由麻省总医院(Massachusetts General Hospital)与布列根妇女医院(Brigham and Women's Hospital)共同创建的非营利性学术医疗系统,也是哈佛医学院的主要教学附属机构。

据了解,麻总百瀚每年科研投入超过 20 亿美元,拥有逾 8 万名员工,服务超过 250 万患者,是美国最大医院型科研机构。其旗下包括麻省眼耳医院、麦克林精神病中心、Spaulding 康复医院等在各自领域名列前茅的专科机构,历史上曾孕育出 22 位诺贝尔奖获得者,体现了该系统在全球医学研究版图中的顶级地位。
今天聚焦的这项端粒研究,即由该系统中的布列根妇女医院与佐治亚医学院分子遗传学研究团队共同牵头完成。
Part 1
端粒,人体老化的“倒计时钟”
端粒(telomere)由重复的 DNA 序列构成,分布于染色体两端,如同保护性封套,防止基因组在复制过程中发生信息丢失或染色体融合。
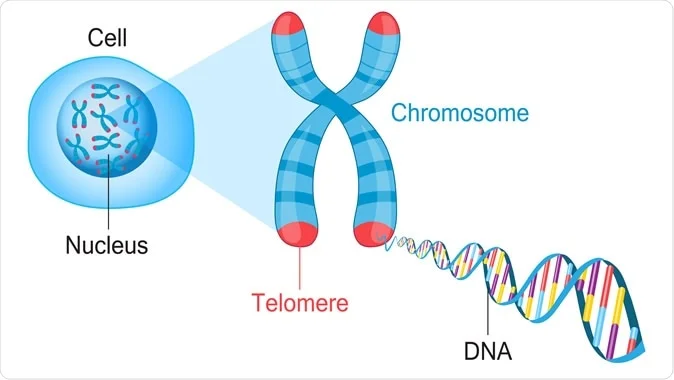
随着细胞分裂次数增加,端粒逐步缩短,最终触及临界长度后细胞将进入衰老或凋亡状态。
这一过程被认为与心血管疾病、糖尿病、癌症及认知退化等多种老年相关疾病的风险上升存在高度的相关性。
在这一背景下,维持或延缓端粒缩短,被视为抗衰老干预的重要方向。
而维生素 D 和 ω-3 脂肪酸因其抗炎、调节免疫等生理作用,长期被推测与端粒功能存在相关性。
然而,现有研究多为短期、小样本干预或横断面观察,结论不一,缺乏长期大样本的临床验证。
Part 2
VITAL 研究首次大规模实证
维生素 D 的端粒保护作用
VITAL(VITamin D and OmegA-3 TriaL)是一项设计严谨的长期临床试验,采用 2×2 因子设计,纳入超过 25000 名美国志愿者,随机分组接受每日 2000 IU 维生素 D3、1g ω-3 脂肪酸、两者联合或安慰剂干预,为期五年。
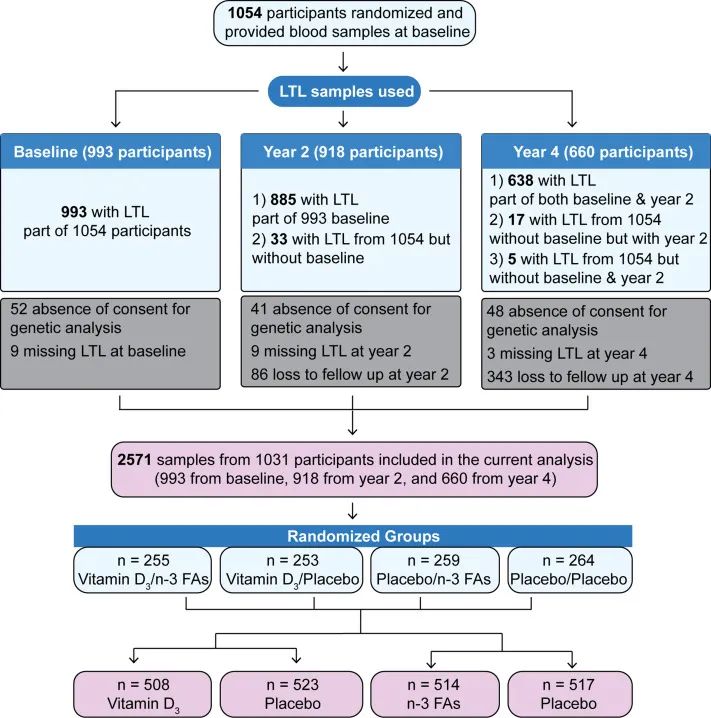
此次端粒子研究纳入其中 1054 名受试者,分别在基线、第 2 年、第 4 年采集白细胞样本,采用定量 PCR 方法检测端粒长度变化。
结果显示,维生素 D3 补充组相比安慰剂组,在 4 年期间减少了平均 140 个碱基对的端粒损耗,约等于延缓了近 3 年的生物老化过程。
每年端粒长度保留增幅达 0.035 kb(p=0.037),具有统计学显著性。而 ω-3 脂肪酸单独补充并未对端粒长度产生显著影响。
这是迄今样本量最大、随访时间最长的双盲 RCT,首次提供维生素 D₃ 减缓人类端粒缩短的高质量证据,表明了其在干预细胞老化路径上具有潜力。
Part 3
维生素 D 如何减缓端粒缩短?
维生素 D 在体内不仅是钙磷代谢调节因子,更参与免疫调控、抗氧化应激与细胞分化等多项生物过程。

观察性研究提示,血清维生素 D 水平偏低往往伴随慢性炎症和 hs-CRP 升高,并可能与端粒酶活性较低相关,但目前仍主要限于相关性证据。
VITAL 研究的前期分析亦发现,补充维生素 D 可在两年内使 hs-CRP 水平下降 19%,提示其可通过抗炎机制减缓端粒损耗。炎症状态被认为是端粒加速缩短的主要推动因子之一,通过调动氧化应激反应、激活细胞凋亡通路、甚至影响端粒酶(telomerase)表达,使细胞更快走向衰老。
体外实验显示,维生素 D 的活性形式 1,25-二羟维生素 D 可能通过调控 hTERT 启动子等途径影响端粒酶活性,其具体方向依细胞类型而异,机制尚待阐明。VITAL 研究在人群层面首次观察到维生素 D3 可减缓端粒缩短,为探索上述机制提供了流行病学线索,
Part 4
预防慢病,从“延缓细胞老化”出发
端粒缩短不仅与自然老化相关,还与癌症、自身免疫疾病等老年慢性病的发病风险上升密切相关。
此次研究中,维生素 D3 干预群体虽未直接分析疾病终点,但其在主研究中已被证实具备一定的慢病预防效应。
在整个 VITAL 研究中,维生素 D3 补充组比安慰剂组发生晚期癌症(转移性或致死性癌症)风险下降 17%;自身免疫疾病(如类风湿关节炎、红斑狼疮等)发病率下降 22%。这与本次端粒保护作用的发现形成生物学上的一致性——端粒缩短的减缓可能与维生素 D 降低疾病风险的生物学机制存在关联。
尽管 ω-3 脂肪酸具备抗炎特性,此次研究未发现其对端粒长度有显著影响。这或许与其抗炎作用机制不同、干预剂量或时间不足有关,也提示维生素 D 可能在细胞老化通路中扮演更核心的角色。
Part 5
行业视角
精准补充趋势下的新兴路径
维生素 D3 的端粒保护作用若在后续研究中进一步验证,将为营养干预与抗衰老产业打开新赛道。
在全球抗老化补充剂市场中,维生素类产品份额较高,但目前主流卖点仍集中在骨骼与免疫支持。
本研究成果则为其赋予了“细胞级别抗衰”的科学基础,或将在配方开发、功能声称、品牌传播等层面催生新的创新方向。
值得注意的是,该研究使用的维生素 D3 剂量为每日 2000 IU,虽高于一般人群膳食推荐摄入量(RDA),但符合国际上多数研究建议的补充范围。这一剂量的选择也提示未来产品设计中应更加注重精准剂量、个体差异与长期安全性评估。
研究团队明确指出,本次研究主要集中在美国中老年人群(平均年龄 65 岁、84% 白人)中进行,结果的普适性尚需在更广泛人群中验证,尤其是在亚洲、非洲等不同遗传背景与生活方式群体中。
此外,端粒长度的变化是否真正转化为临床事件风险的下降,还需更长期追踪数据佐证。未来的研究应尝试将端粒变化与认知退化、心血管事件、癌症发生率等具体临床终点进行联动分析。

在抗衰老机制仍充满未知的当下,这项新研究为维生素 D3 赋予了超越传统功能的科学想象空间。
尽管全面延缓衰老需多维策略,但从端粒切入的探索,或许能重新定义微量营养素在健康老龄化的角色。
参考资料:
Haidong Zhu, JoAnn E. Manson, Nancy R. Cook, Bayu B. Bekele, Li Chen, Kevin J. Kane, Ying Huang, Wenjun Li, William Christen, I-Min Lee, Yanbin Dong. Vitamin D3 and Marine Omega-3 Fatty Acids Supplementation and Leukocyte Telomere Length: 4-Year Findings from the VITAL Randomized Controlled Trial. The American Journal of Clinical Nutrition, 2025; DOI: 10.1016/j.ajcnut.2025.05.003
DNA methylation closely linked to telomere length - News-Medical
来源:![]()
作者:John Xie

