荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
在癌症治疗领域,科学家们一直在探索肿瘤微环境的机械特性如何影响癌症的发展。近日,美国德克萨斯农工大学(Texas A&M University)研究团队在《自然通讯》(Nature Communications)期刊上发表重要研究成果,揭示了肿瘤细胞核的力学特性与癌症进展之间的关系,为开发新型抗癌疗法提供了全新思路。
Part 1
细胞核力学特性研究取得重要突破
据世界卫生组织数据显示,2022 年全球新增癌症病例超过 2000 万,死亡病例近 1000 万。这些数字令人警醒,科学家们正在微观层面寻找治疗突破口。
德克萨斯农工大学生物医学工程系的 Samere Zade 和化学工程系的 Wang Ting-Ching 领导的研究团队,通过深入研究肿瘤细胞核的结构和功能变化,发现了一个关键的生物力学机制。

这项研究的主要发现在于,肿瘤细胞所处微环境的硬度变化会直接影响细胞核的形态和功能。
研究人员发现,当细胞处于较硬的环境中时,细胞核的层纤结构(nuclear lamina)会发生显著变化,从皱褶状态变为紧绷状态。这种变化会促使一种称为 YAP(Yes 相关蛋白)的关键蛋白质向细胞核内迁移,从而刺激细胞增殖。
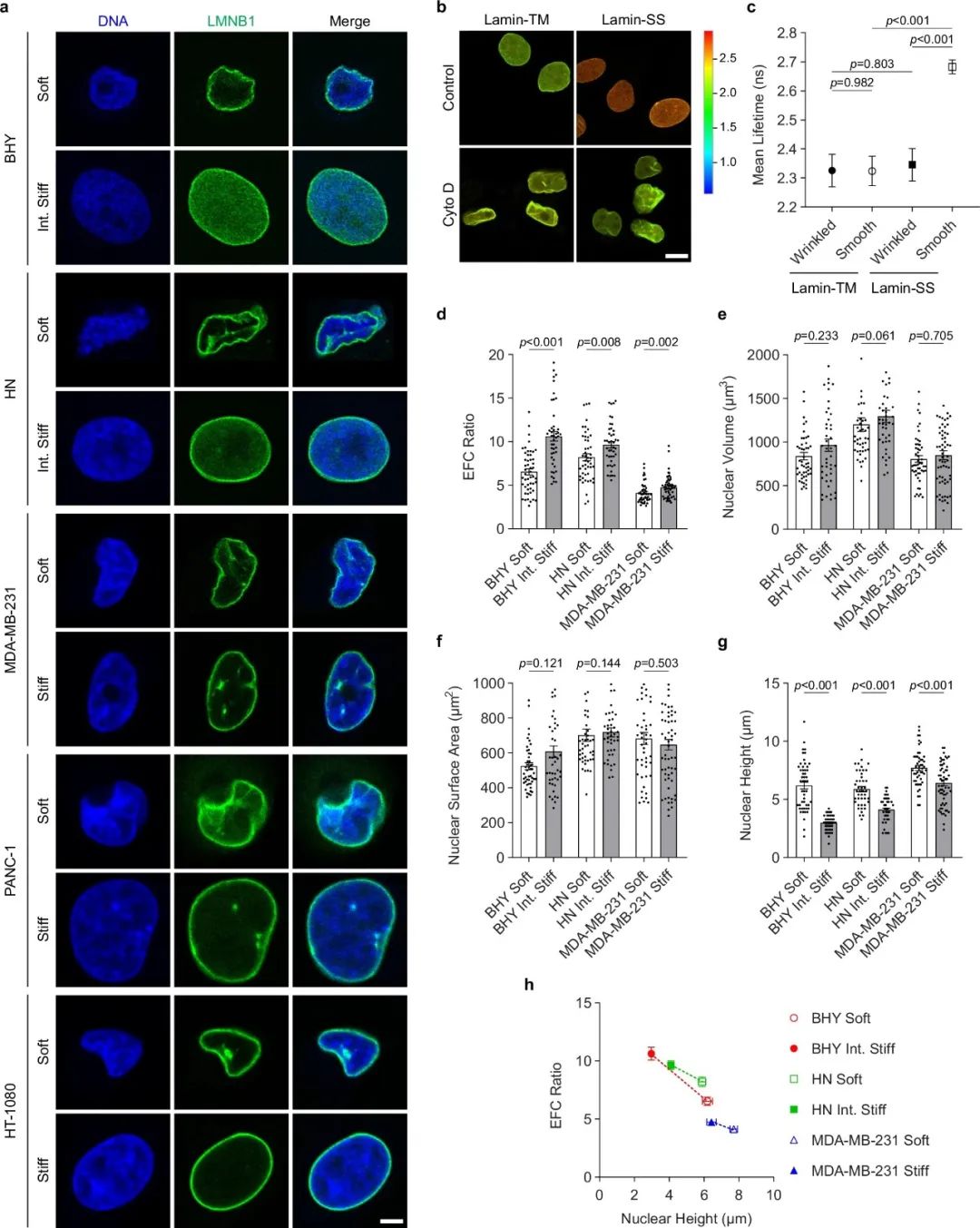
图:细胞外基质(ECM)硬度调控细胞核的皱褶特性
研究团队的共同负责人、生物医学工程和化学工程系教授 Tanmay Lele 指出,癌症一直是一种难以治疗的疾病,它极其复杂,而且促进肿瘤发展的分子机制尚未完全阐明。这项研究发现为理解肿瘤组织硬化如何促进肿瘤细胞增殖提供了新的见解。
这项研究的创新之处在于首次揭示了细胞核的液滴模型(nuclear drop model)在肿瘤发展中的作用。研究人员发现,细胞核的层纤结构表现出独特的力学阈值行为:一旦展平,层纤结构就会呈现出不可延展的特性。通过计算机模拟和实验验证,研究团队证实,当细胞在硬基质上铺展时,细胞核变平导致层纤结构展开并产生张力。
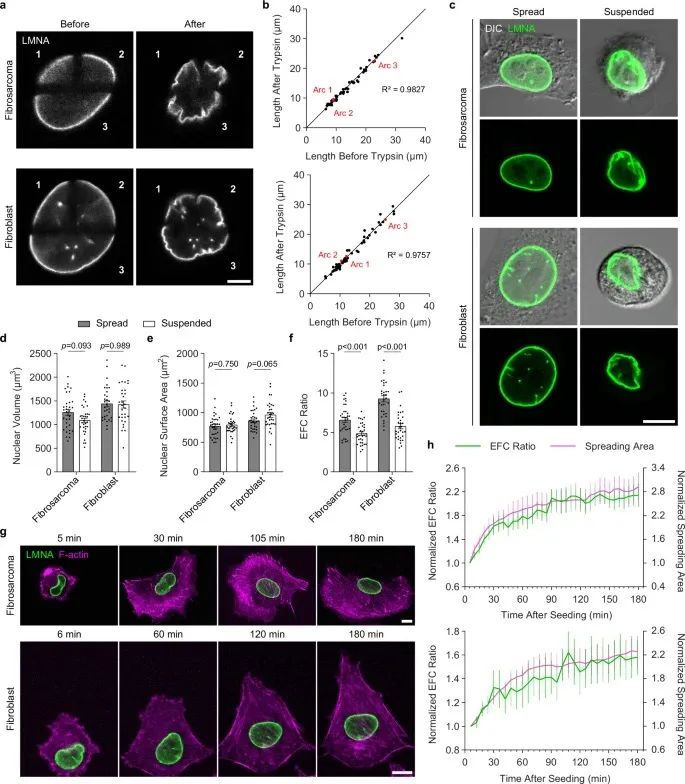
图:细胞核层纤结构的皱褶动态变化由细胞圆化或铺展驱动
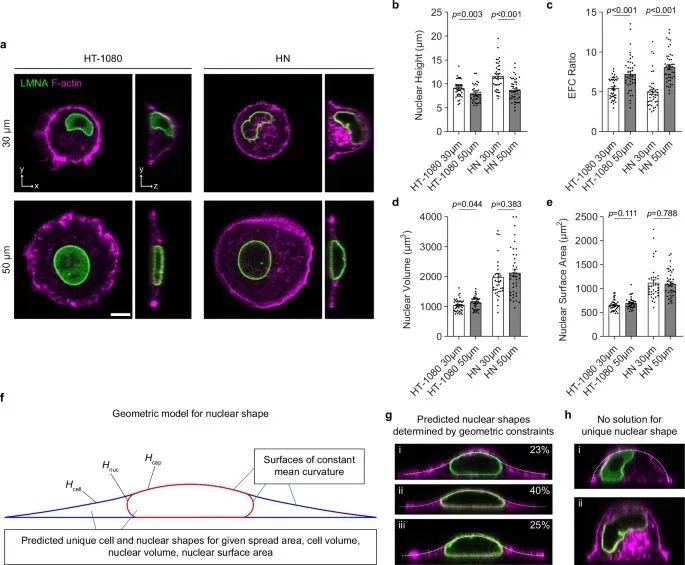
图:核液滴模型对细胞核极限形态的定量预测
更为重要的是,研究人员发现,一种称为 lamin A/C(核纤层蛋白A/C)的蛋白质在这一过程中发挥着关键作用。降低 lamin A/C 的水平会减少 YAP 向细胞核的定位,从而抑制细胞的快速增殖。这一发现为开发针对性治疗策略提供了新的靶点。
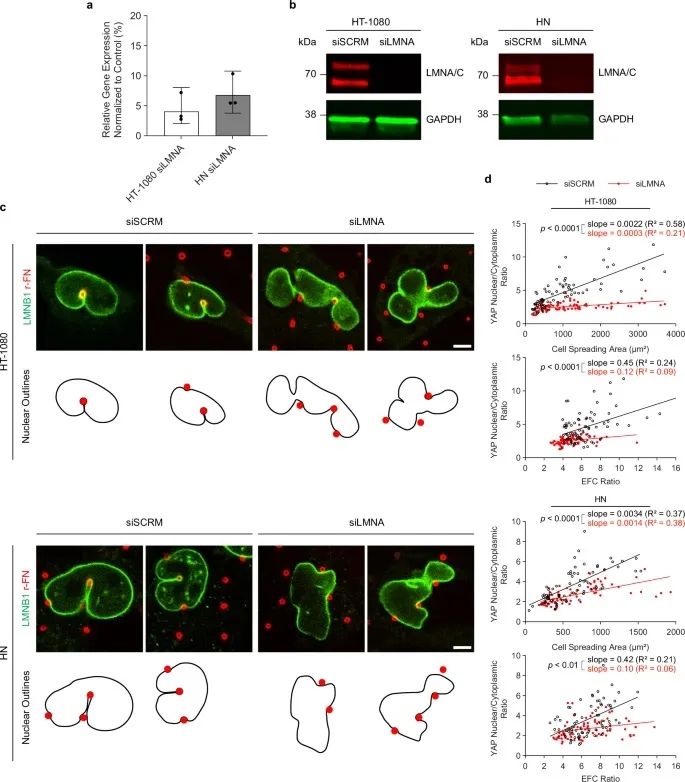
图:核纤层蛋白 A/C 对层纤结构表面张力以及 YAP 对层纤结构展开和细胞铺展的敏感性是必需的
了解基质硬度如何驱动细胞核变化并调节关键信号通路,例如 YAP 信号通路,将为开发针对这些力学通路的治疗方法打开了新的大门。可以设计药物或治疗方法来软化肿瘤环境,干扰帮助癌细胞生长的物理信号。lamin A/C 及相关的细胞核力学特性可能成为癌症治疗的新靶点。
Part 2
创新技术揭示多种癌症共同特征
研究团队采用了多种创新技术手段,包括荧光共振能量转移(FRET)技术、高分辨率显微成像以及计算机模拟等,对五种不同的癌细胞系进行了系统研究。他们发现,这种细胞核力学特性的变化在多种癌症类型中都普遍存在,包括口腔鳞状细胞癌、乳腺癌、胰腺癌和纤维肉瘤等。
该研究还揭示了一个重要现象:在三维培养环境中,癌细胞的核形态与二维培养条件下有显著差异。研究团队使用明胶甲基丙烯酸酯(GelMA)水凝胶进行实验,发现在软性凝胶(1-3 kPa)中,细胞呈现出延长状态,细胞核层纤结构处于紧绷状态;而在硬性凝胶(10-15 kPa)中,细胞则呈现圆形,细胞核层纤结构出现皱褶。这一发现对于理解真实肿瘤环境中的细胞行为具有重要启示。
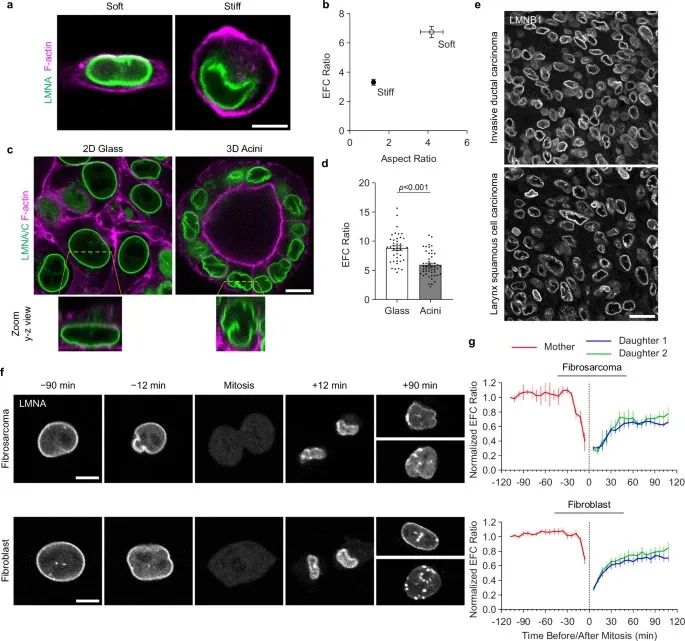
图:三维培养中的层纤结构皱褶对硬度敏感,并在有丝分裂后形成
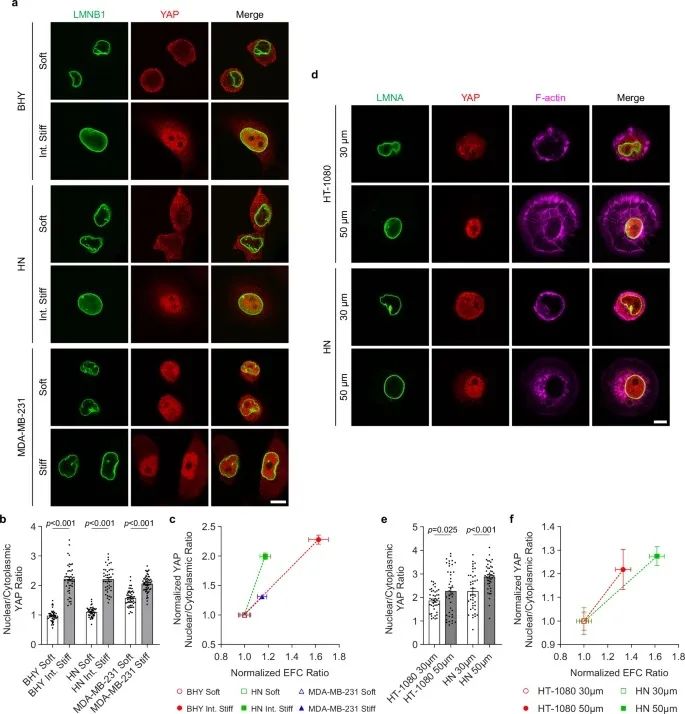
图:层纤结构的皱褶与 YAP 核定位呈负相关
德克萨斯农工大学的研究团队目前正在进一步探索这些发现在临床患者来源的肿瘤样本中的应用。这项研究获得了美国国立卫生研究院(NIH)、德克萨斯州癌症预防和研究所(CPRIT)以及美国国家科学基金会(NSF)的资助。
Part 3
研究发现为抗癌药物开发指明新方向
值得注意的是,这项研究成果为开发新型抗癌药物提供了多个潜在方向:
首先,开发能够调节细胞核力学特性的药物,特别是针对 lamin A/C 蛋白的调节剂;
其次,研究能够改变肿瘤组织硬度的治疗方案,从而影响癌细胞的增殖行为;
第三,探索 YAP 信号通路的调控机制,开发相关的靶向治疗策略。
这项研究深化了对癌症发展机制的理解,也为药物研发提供了新的思路,有望看到更多基于细胞核力学特性的创新疗法出现。
参考文献:
Wang, T., Abolghasemzade, S., McKee, B. P., Singh, I., Pendyala, K., Mohajeri, M., Patel, H., Shaji, A., Kersey, A. L., Harsh, K., Kaur, S., Dollahon, C. R., Chukkapalli, S., Lele, P. P., Conway, D. E., Gaharwar, A. K., Dickinson, R. B., & Lele, T. P. (2024). Matrix stiffness drives drop like nuclear deformation and lamin A/C tension-dependent YAP nuclear localization. Nature Communications, 15(1), 1-17. https://doi.org/10.1038/s41467-024-54577-4
作者:John Xie

