荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
丛集性癫痫发作/急性反复性癫痫发作在我国癫痫患者中普遍存在,但因为医疗资源不足和对癫痫的认知缺失,使得许多患者不能得到及时有效的治疗。近期,康哲药业的地西泮鼻喷雾剂新药上市许可申请(NDA)获中国国家药品监督管理局(NMPA)批准,成为中国首个地西泮鼻喷雾剂,用于六岁及以上儿童和成人癫痫患者的丛集性癫痫发作/急性反复性癫痫发作的急性治疗,或能为这个治疗缺口提供一种新的解决方案。
根据临床诊疗指南癫痫病分册(2023年修订版),丛集性癫痫发作/急性反复性癫痫发作的定义指成人24小时内(儿童12小时内)出现3次或3次以上发作(发作间歇期等于或小于8小时),且两次发作之间意识恢复正常水平。丛集性发作常见于某些癫痫综合征、月经期癫痫发作及药物难治性癫痫等,如不及时治疗,部分将会演变为癫痫持续状态,危及患者生命。
据估算,中国约640万活动性癫痫患者,每年约30万新发患者,但由于人们对癫痫缺乏正确认识以及医疗资源匮乏,中国目前活动性癫痫患者仍存在约49.8%的治疗缺口,约300万活动性癫痫患者未得到合理治疗。目前国内尚缺乏对于丛集性癫痫发作的流行病学研究,根据海外研究,丛集性癫痫发作的门诊发病率约为15%,由此估算中国接受正规治疗的活动性癫痫患者中,有近50万癫痫患者仍存在丛集性癫痫发作。
2018年时,康哲药业通过其全资附属公司与集团CEO林刚先生全资持有的A&B(香港)有限公司签订了有关含有NRL-1(鼻内地西泮)等和/或延伸线,A&B从某实体处获得资产,该实体又从Neurelis, Inc.处获得资产。

Neurelis是一家私人控股的专业制药公司,位于圣地亚哥,旨在为癫痫和更广泛的中枢神经系统(CNS)市场提供许可、开发和商业化候选产品。Neurelis利用其在CNS化合物开发和商业化方面的专业知识以及与这些市场领先的研究人员和临床医生的密切关系,推动独特的候选产品,如NRL-1,用于治疗急性重复或丛集性癫痫发作,以解决重大未满足的医疗问题需要。
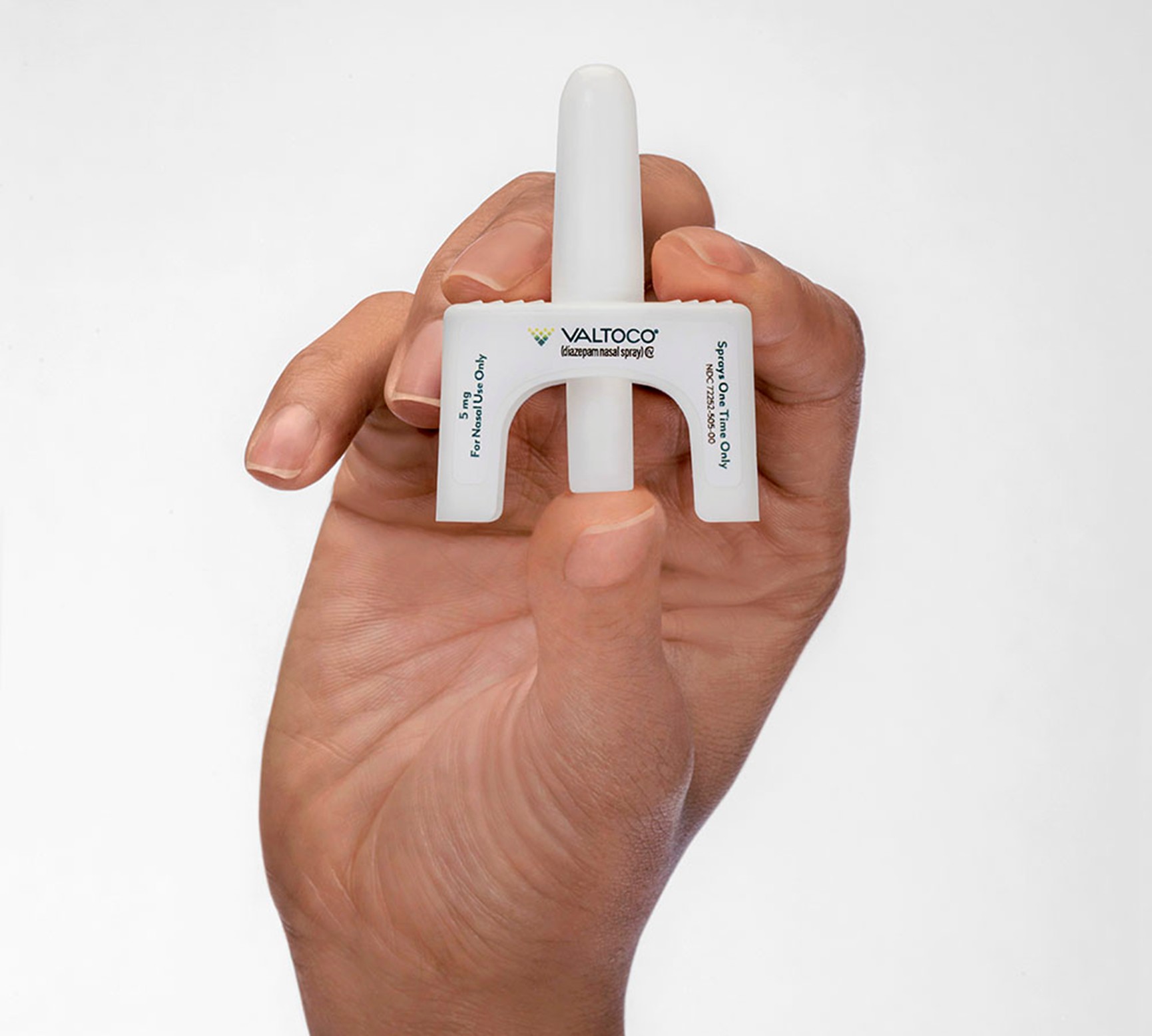
在2020年,美国食品和药物管理局(FDA)批准了Neurelis的NRL-1,即Valtoco(地西泮鼻腔喷雾剂)作为一种急性治疗药物治疗6岁及以上癫痫患者的间歇性、刻板性癫痫频繁发作活动(即癫痫丛集)。

Valtoco是一种专利配方的diazepam(地西泮),融入了一种基于维生素E的溶液和Intravail®吸收增强技术的独特组合。在批准之前,FDA已授予Valtoco孤儿药地位和快速通道地位。Intravail®经粘膜吸收增强技术可以无创性地输送多种蛋白质、肽和小分子药物。
Valtoco的批准得到了广泛的临床和临床前研究的数据支持,包括在健康志愿者和癫痫患者中开展的研究。在一项长期、开放标签、重复给药的患者研究中,对Valtoco的安全性进行了评估:共入组130多例患者,超过2000次癫痫发作采用Valtoco进行了治疗。研究中,Valtoco表现出了高的生物利用度,每次给药之间的变化度低,并且安全性和耐受性良好,最常见的不良反应(≥4%)为嗜睡、头痛和鼻不适。
康哲药业在Neurelis向美国FDA递交新药申请后,就在中国积极开展VALTOCO的注册申请等相关工作,随后获得了中华人民共和国国家药品监督管理局对地西泮鼻喷雾剂的临床试验通知书,开展针对中国人群的比较药代动力学研究,在药品申请注册上市的同时提交上市后进一步验证本品疗效及安全性的临床研究计划。
此次这款新药在6月7日获得NMPA批准,成为了中国第一款获批用于丛集性癫痫发作的药物。在医生的处方及医护人员指导下,患者或其照顾者可及时地通过鼻内给药途径,随时随地施用,能够满足目前国内癫痫患者丛集性癫痫发作时,急性治疗的临床需求通过鼻内给药。
参考资料:
NEURELIS ANNOUNCES COMMERCIAL AVAILABILITY OF VALTOCO® (DIAZEPAM NASAL SPRAY) FOR SEIZURE CLUSTER RESCUE
NEURELIS ANNOUNCES FDA APPROVAL FOR SEIZURE RESCUE TREATMENT VALTOCO® (DIAZEPAM NASAL SPRAY) THAT INCORPORATES THE SCIENCE OF INTRAVAIL® FOR CONSISTENT AND RELIABLE ABSORPTION
自願性及業務進展公告-地西泮鼻噴霧劑中國新藥上市申請獲批