荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
一、九大衰老诱因
衰老是随着时间推移产生的一种生存和生育所必需的生理功能退化,具体表现为生理完整性的逐渐丧失和器官功能受损。衰老细胞,也被称为僵尸细胞,是细胞进入一种不可逆的周期停滞状态,细胞彻底失去了增殖能力,持续分泌出各种细胞因子和蛋白酶等,传染周围的细胞,或者损伤细胞的正常结构。衰老的主要标志是:基因组不稳定、端粒损耗、表观遗传改变、蛋白质稳态丧失、营养感应失调、线粒体功能障碍、细胞衰老、干细胞耗竭和细胞间通讯改变1等(图一)。
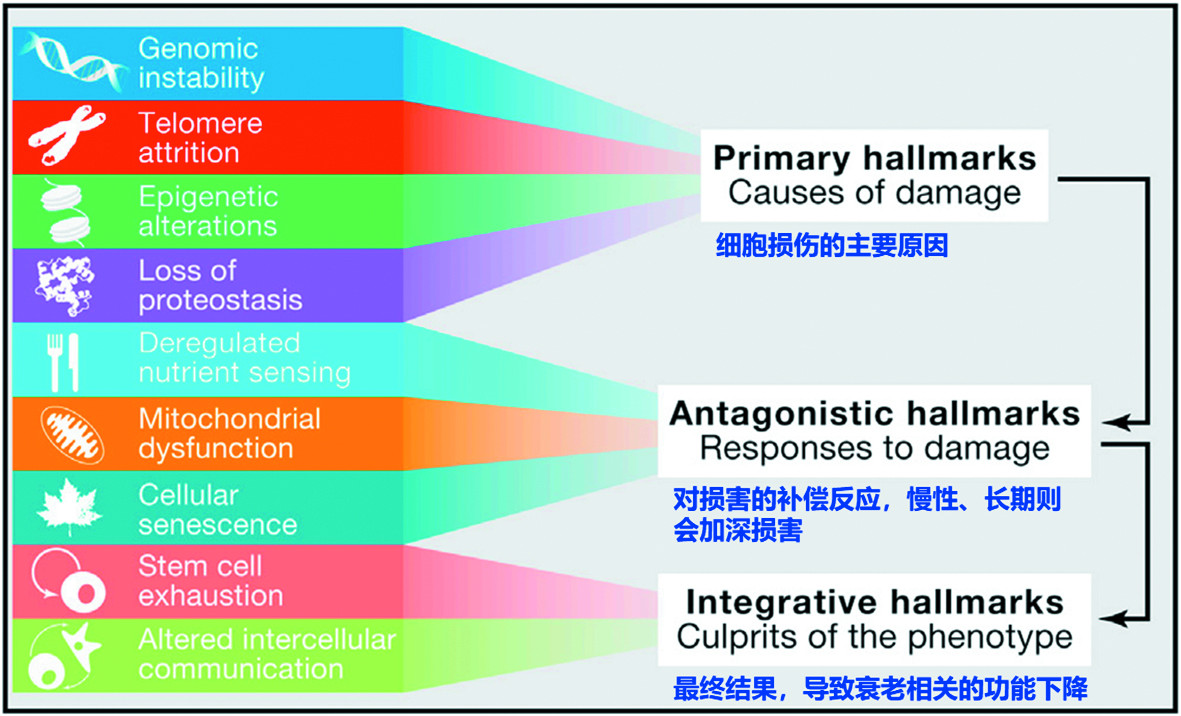
图一. 衰老的主要标志
图片来源 (PMID: 23746838)
1.基因组不稳定
衰老的一个共同点是基因损伤促使富集DNA 的完整性和稳定性不断受到外源性物理、化学和生物因素威胁,以及内源性威胁,包括 DNA 复制错误,自发水解反应和活性氧(ROS)。这种内因或者外因导致的遗传病变是高度多样化的,包括点突变、易位、染色体缺失,端粒缩短和由病毒整合或转座子引起的基因突变2。

2.端粒损耗
随着年龄的增长,DNA 损伤似乎会随机发生在基因组的某一位置。但有一些染色体区域,如端粒,特别容易受到与年龄相关的影响。DNA 复制酶缺乏复制完整线性DNA分子末端的能力,而端粒酶具有这个能力。然而,大多数哺乳动物的体细胞并不表达端粒酶,所以经过几代复制,会导致染色体端粒保护序列丢失,这也解释了某些类型细胞在体外培养时增殖能力有限的问题3。
3.表观遗传改变
在整个生命过程,各种各样的表观遗传改变影响着机体所有细胞和组织。表观遗传改变包括 DNA 甲基化模式的改变,翻译后组蛋白修饰和染色质重塑。升高的组蛋白 H4K16乙酰化,H4K20三甲基化,或H3K4三甲基化,以及降低的H3K9甲基化或 H3K27三甲基化,构成了衰老相关的表观遗传基本特征。这种多酶促系统,包括 DNA 甲基转移酶,组蛋白乙酰化酶、脱乙酰酶、甲基化酶和去甲基化酶,以及涉及染色质重塑的蛋白质复合物,保证和维持了表观遗传模式4。
4.蛋白质稳态丧失
衰老和一些与衰老相关的疾病与受损的蛋白质稳态有关。所有细胞都利用了一系列质量控制机制来保持其蛋白质组的稳定性和功能性。蛋白质稳态涉及保证其正确及稳定折叠的蛋白质——最常见的是热休克蛋白家族中蛋白酶体和溶酶体对蛋白质的降解作用5。
5.营养感应失调
哺乳动物的生长激素轴包括由垂体前叶产生的生长激素。许多细胞可以被生长激素刺激,产生生长激素调节剂胰岛素样生长因子 1 (IGF-1),最显着的是肝细胞。当细胞内有葡萄糖时被激活,IGF-1的细胞内信号通路就像胰岛素信号通路一样。 因此,IGF-1 和胰岛素信号被叫做作为“胰岛素和 IGF-1 信号”(IIS) 通路。 值得注意的是,IIS通路是进化过程中最保守的由衰老控制的通路。在它的多个靶点中, FOXO 家族转录因子和 mTOR 复合物参与调控老化过程。限制 GH、IGF-1 受体,胰岛素受体表达,或控制下游细胞内效应器功能(如AKT、mTOR 和 FOXO)的突变,可以抗衰老6。
6.线粒体功能障碍
随着细胞和生物体的老化,呼吸链的效率降低,从而导致电子丢失和ATP 减少。线粒体功能障碍和衰老之间的关系长期以来都在被讨论,但有些细节仍然有待考究。线粒体自由基理论指出,随着细胞衰老,细胞发生程序性、进行性线粒体失调,导致 ROS 的产生增加,反过来造成线粒体功能障碍和细胞损伤。也有报告指出说,线粒体功能障碍导致的衰老可以不需要ROS 参与,但这个过程可能涉及到多条信号途径。例如,线粒体功能缺陷可能会导致线粒体膜的通透性增加,方便ROS活化的炎症小体进出线粒体,从而影响细胞凋亡7。
7.细胞衰老
细胞衰老的描述是在人成纤维细胞的连续传代时首先观察到的。而今天,我们知道那时观察到的衰老是由端粒缩短引起的。但是,还有很多其他的因素也可以导致衰老。最值得注意的是,非端粒 DNA 损伤和INK4/ARF基因座的去抑制,这两者都发生在老化过程中,也能够诱发衰老。DNA 损伤和β-半乳糖苷酶 (SABG) 通常被用来鉴定组织中的衰老细胞。 我们认为当细胞损伤变得有害时,这些有害的细胞需要被清除,此时细胞衰老是一件有益的事情,但是当组织细胞耗尽其再生能力时,会加速衰老8。
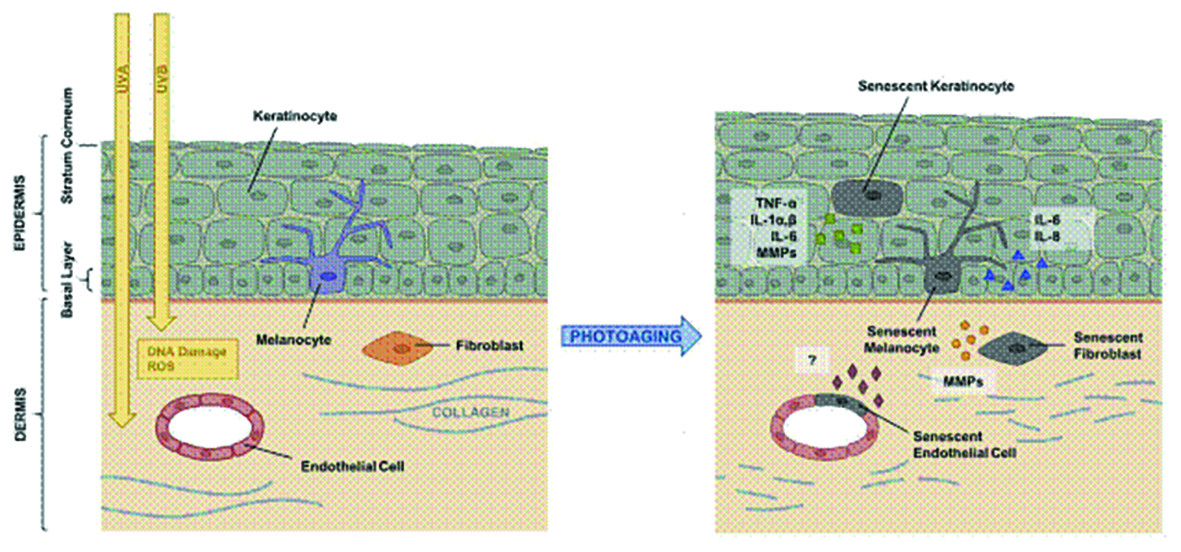
图二 UVA 和UVB 诱导的不同种类的皮肤细胞衰老
图片来源(PMID: 33349436)
8.干细胞耗竭
衰老的最明显特征之一就是组织再生能力的下降。 例如,造血功能随着年龄的增长而下降,导致适应性免疫细胞减少的过程叫免疫衰老。这与DNA 损伤的积累和细胞周期抑制蛋白的过度表达有关。端粒缩短也是干细胞衰退的重要原因。特别是,mTORC1 抑制雷帕霉素,可以通过改善蛋白质稳态来延缓衰老,也可能改善表皮、造血系统,肠道中的干细胞功能。干细胞衰竭是多种原因导致的老化相关损害造成的综合结果,并可能是导致组织和机体老化的罪魁祸首之一9。
9.细胞间通讯改变
除了细胞自主改变,衰老还涉及细胞间通讯水平的变化,无论是内分泌还是神经元。 因此,在衰老过程中,神经激素信号(例如,肾素-血管紧张素、肾上腺素、胰岛素-IGF1 信号)会随着炎症反应的增加而失调,针对病原体和癌前细胞的免疫监视会下降,以及细胞周围和细胞外环境的组成变化。由细胞间通讯变化导致的衰老,其中一个明显的特点是“炎症性的”10。
二、皮肤老化的分类、原因及抗老化靶点
皮肤老化一般可以分为两类:(一)内源性老化(也叫慢性老化):内源性老化是受基因控制的在有机体内自然发生的一个不可逆过程。 内源性老化的快慢取决于个体遗传时钟,并受到自身自由基清除能力和修复能力的影响。内源性老化主要发生部位很少直接暴露于外界环境(如阳光,环境污染物等);(二)外源性老化 (也叫光老化): 光老化是指皮肤长期暴露于阳光紫外线造成皮肤的加速老化。 光老化的皮肤表现为表皮变厚,皮肤干燥,皱纹加深,皮肤失去弹性,伤口愈合延迟,也会有发展成皮肤癌的风险11。这里我们重点讲述光老化的原理。
紫外线包含三类: UVA(320-400 nm), UVB (280-320 nm), UVC(100-280nm),其中UVC 和大部分UVB在大气层中被吸收,绝大部分UVA (~95%)和剩余小部分UVB(~5%) 会穿越大气层到达地球。尽管到达地面的UVA 占绝大部分,但是UVB 却是造成晒伤的罪魁祸首。因为UVB波长短,能量高,绝大部分会被表皮层吸收,少部分仍会穿过表皮到达真皮层。 相反,UVA 能够穿过表皮层到达真皮层,现在被认为是造成皮肤老化和黑素瘤的原因。 UVA 和UVB 都能够刺激产生有破坏性的ROS 来直接造成DNA 损伤,导致老化。综上所述, UVA 和 UVB 都是造成皮肤老化, 黑素瘤和皮肤癌最主要原因11 (图二)。
光老化信号通路及靶点
1.ROS/MAPK/AP-1
紫外线可以诱导产生ROS, ROS 可以活化丝裂原活化蛋白激酶(MAPKs)信号通路, 包括细胞外信号调节激酶 (ERK),P38和氨基末端激酶(JNK)。这些激酶能够激活下游的转录活化蛋白1(AP-1)包括c-Jun 和c-Fos。AP-1 能够促进基质金属蛋白酶类的表达。 这类酶主要是角质细胞在紫外线的诱导下产生的,能够裂解胶原蛋白和弹性蛋白,导致皮肤失去弹性,失去支撑结构,皱纹加深12。
2.NF-κB
UV诱导ROS的产生, 过多的ROS激活NF-κB信号通路和MAPK信号通路,促进NF-κB和AP-1和的激活, 进而提高了TNF-α的水平和MMPs的表达,从而诱导细胞外基质的降解并加速皮肤老化。许多信号通路都会涉及到NF-κB 的激活,例如胰岛素/IGF-1信号会激活 PI- 3K/AKT,PI-3K/AKT 信号反过来激活 NF-κB;激活哺乳动物雷帕霉素靶标 (mTOR) (应激反应的介质,促衰老因子)同样可以激活NF-κB。 此外,炎症、应激通路和DNA损伤等过程也是最终通过激活 NF-κB 信号从而加速老化。此外,端粒缩短是公认的衰老标志,会导致基因组不稳定, 也是通过并通过激活 NF-κB 和增加 COX-2 和 ROS(活性氧)水平来促进衰老。总之,很多种不同的信号通路可以加速细胞衰老,这些信号通路同时也激活了NF-κB 信号,NF-κB 反过来通过诱导细胞衰老、促进衰老相关分泌表型(SASP)、凋亡信号和炎症反应13。
3.SIRT长寿基因
如 SIRT(调节寿命的 sirtuin 家族的 II 类组蛋白脱乙酰酶成员 ),会抑制 NF-κB 信号。SIRT1 和 SIRT6,直接与 p65 相互作用,抑制 NF-κB 的转录活性,从而减缓光老化14。
4.黑色素细胞在于表皮层,产生黑色素,几乎不分裂增殖。在紫外线的诱导下,黑色素产量增加,转移到角质细胞处帮助吸收紫外线,保护胶质细胞,避免造成DNA 损伤。p53 是众多调控黑色素生成的酶之一。UVB 造成的活化,过度表达,造成黑色素增多,皮肤暗黑,色素沉积15。
5.自噬相关蛋白(Belin1, ATG5/12, LC3, p62)
自噬现在被认为是调节皮肤老化的关键因素,因为它在维持皮肤健康方面起着重要作用。 自噬可以去除老化的亚细胞器和蛋白质,从而维持细胞内环境稳态。缺乏自噬会导致炎症小体激活引起皮肤过度炎症反应,从而加速衰老16。我们偶然在小鼠皮肤炎症模型中,利用双光子共聚焦显微镜活体成像观测到了细胞自噬的完整过程。
6.Nrf2-ARE
紫外线对皮肤的影响源于ROS的产生。细胞内部本身自带抗氧化系统,包括核因子 E2 相关因子 2 (Nrf2) 和抗氧化反应元件 (ARE) 信号通路。正常状态下,Nrf2 在细胞质; 当有ROS 刺激时,Nrf2 转运进入细胞核与ARE 结合,启动胞内抗氧化酶 (包括NAD(P)H:醌氧化还原酶 1 (NQO-1)、血红素加氧酶 1 (HO-1) 和谷胱甘肽)的合成,从而保护细胞免受ROS 侵害12。
7.TGF-β /SMAD
转化生长因子-β (TGF-β) 是主要促进胶原蛋白生物合成的细胞因子。TGF-β通过调控下游信号SMAD来达到合成胶原蛋白的生物学过程。 UV激活的转录活化蛋白1(AP-1)能够抑制TGF-β/SMAD信号通路,导致光老化。
三、人参皂苷抗老化机理研究
人参早在甲骨文代表作《殷墟书契前编》就有收录,但药用精髓始载于《神农本草经》,谓“人参,味甘微寒。主补五脏,安精神,定魂魄,止惊悸,除邪气,明目,开心益智。久服,轻身延年。一名人衔,一名鬼盖。生山谷”。对此药效经纶,现代学者已经进行了考察验证,确认相关人参医疗作用之记载完全正确。人参核心生物活性成分为人参皂苷,多达182种。普通种植参和野山参的人善皂苷含量差异巨大,这也是为什么野山参药效要比种植参高出很多倍的主要原因。稀有人参皂苷 (包括Rg组,Rh组,Rk组等)在种植参中一般不存在,在老野山参中少量存在, 但是含量极低, 一般为万分之几, 这也是野山参的珍贵的原因18。
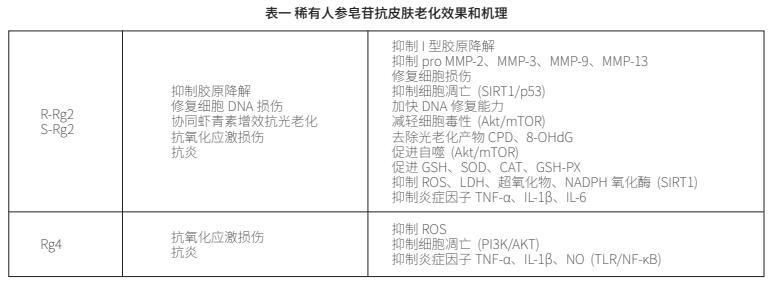
根据实验结果,我们列出了一些稀有人参皂苷在治疗皮肤老化中的作用,也解释了其作用机理。
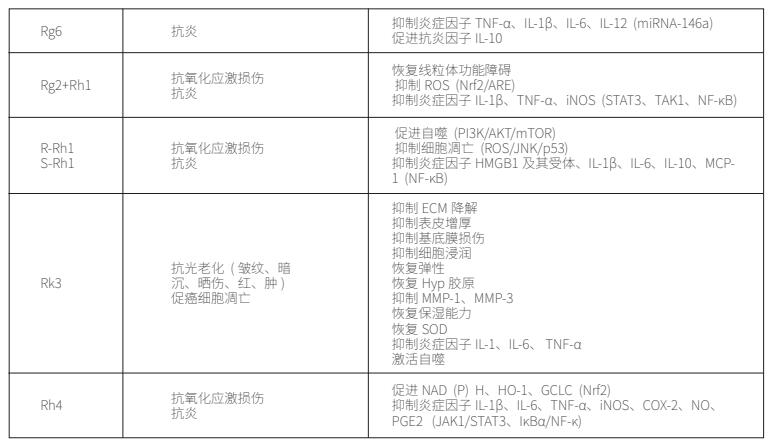
总结
机体衰老是一个不可逆转的过程,无法避免,但是,我们可以通过科学手段来延缓衰老。一直以来关于“百草之王”人参的研究是百花齐放,在抗癌领域的研究更是捷报频传,但是,很少有人关注到人参在抗老化领域的应用。我们期待用科学、准确,严谨的数据把人参在抗老化领域的潜力一一展现给大家。

来源:荣格-《国际个人护理品生产商情》
原创声明:
本站所有原创内容未经允许,禁止任何网站、微信公众号等平台等机构转载、摘抄,否则荣格工业传媒保留追责权利。任何此前未经允许,已经转载本站原创文章的平台,请立即删除相关文章。