荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
近期,日本大阪市立大学的研究人员开发了一种替代免疫测定和其他用于蛋白质分析的光学方法。这种替代方法通过激光照射对蛋白质进行快速、高度敏感的检测。
据研究人员称,这种基于光诱导加速的技术可以提高检测极限和定量测量,使用少量的生物样本和简单的过程,以帮助对癌症、痴呆症和传染病进行超早期诊断。传统的蛋白质检测技术,如酶联免疫吸附试验(ELISA)需要几个小时并涉及多个步骤。此外,这种方法还不如最近开发的光诱导方法敏感。
实验中,研究人员的新方法只用了3分钟的激光照射就成功部署,从而实现了与传统蛋白质检测方法相比超过100倍的灵敏度和超快的特异性检测。此外,研究人员表明,该技术只需少量的体液如一滴血就能进行诊断。
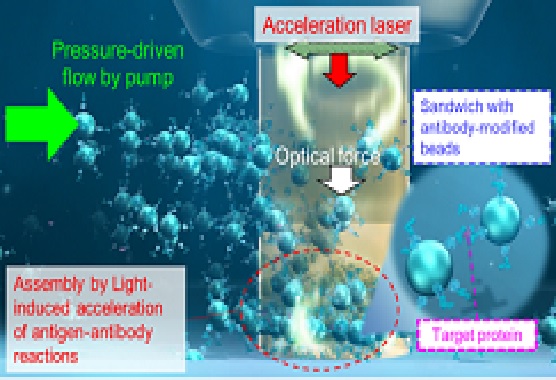
大阪市立大学的研究人员将目标蛋白和具有选择性地与目标蛋白结合的改性抗体的探针颗粒引入一个小通道,并应用红外激光进行照射。首次实现了在仅仅3分钟的激光照射后,快速测量微量的阿克级目标蛋白
为了开发一种光学方法来实现对抗原-抗体反应的控制并检测微量的蛋白质,研究人员对光学压力和流体压力的协同作用以及如何规避热的影响进行了基础研究。他们使用目标蛋白,并向其引入含有选择性地与蛋白结合的改良抗体的探针颗粒。
他们将蛋白质和探针颗粒限制在一个微通道中,并对该通道进行照射。探针颗粒是直径2微米的聚合物珠子,由于吸收红外激光以及强烈的光散射,产生的热量很小。然后,研究人员利用光诱导加速,在固体和液体之间的界面(即通道的底部,其中包含液体样品)捕获了微量蛋白质的抗原-抗体反应。
在将激光照射面积调整到与约束几何结构相当之后,研究人员照射了几百毫瓦的激光,在宽度约为100μm的微通道中散焦到约70μm的光斑大小。蛋白质和探针颗粒上的激光辅助光学压力,增加了相互作用的概率和抗原-抗体反应的加速。目标分子和探针颗粒的碰撞概率通过光力和流体压力得到了增强。
“散射力”是光学力的一个组成部分,增强了散射力可以确保累积力不会对抗体修饰的探针颗粒和靶蛋白造成任何热损伤。在测试各种条件后,研究人员发现,通过将流速调整到100至200微米/秒,抗原-抗体反应被有效加速。
在通过激光照射获得的组装结构的一部分中形成的黑色区域,因为光学透射被多层结构形成阻挡。研究人员发现,该区域的面积与蛋白质浓度呈正相关。使用内聚能表示抗原抗体反应的结合的模型计算从理论上证实了多层结构的形成是由光学力和压力驱动流引起的。
当研究人员用红外激光照射微通道3分钟后,他们能够检测到微量的蛋白质,其灵敏度比传统的蛋白质检测高出约100倍。研究人员实现了对几十阿克(ag)(ag=10-18克;万亿分之一克)数量级的微量的快速测量。仅仅经过3分钟的激光照射,他们就测出了小至二十万亿分之一克的目标蛋白痕量。
研究人员将光诱导加速原理应用于几种不同类型的膜蛋白。在实验中,光学技术显示了对目标蛋白的超快、特异性检测,与传统技术相比,其样本体积更小,灵敏度更高。例如,在一种类型的膜蛋白中,研究人员在没有任何预处理的情况下,在激光照射仅3分钟后,从300 nL的样品中检测到47至750阿克的靶蛋白。
作为日本科学技术厅未来社会创建项目的一部分,正在进行一项利用患者来源样本进行癌症标志物测量的渐进式合作研究。研究人员表示,计划在临床实践中对光诱导加速技术进行初步验证,目的是在几年内开发出一个基本系统。
由于抗原抗体反应是一种常见的生化反应,因此该技术不仅有可能用于医疗领域,也有可能用于各种工业领域,例如测试食品和饮料中的过敏原,检测环境中的生物物质,以及测试制药过程中的中间产品。