荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
● COVID-19如何永久改变制药业生态?
● 2021年10款‘重头药’的审批将如何?
● HPAPI(高效原料药)市场将达330亿美元!
● 制造趋向小规模、模块化;
● 无菌生产,现有法规难以解决行业的争论不休?
● 冷链需求终将从深冻回归冷藏;
● “细胞银行”成为机遇、利基药物受到青睐;
● 占全球经济产出60%的产品将能够通过生物手段来生产,生物制药革命扎根;
默克、密理博、辉瑞、路博润、Cryoport Systems、Recipharm、艾万拓、Rubius Therapeutics、高思、MasterControl QMS、麦肯锡、Evaluate、安永.......
从药物研发、制造技术、新规监管,
到创新疗法、终端市场格局,
我们采集了制药行业“领头羊”们的观点,
他们预测的2021年整个行业的关键趋势。
创新疗法
1. 10款‘重头药’的审批
2.“T细胞银行”业务将迎来巨大机会
3. 继续青睐利基药物
1. 2021年10款‘重头药’的审批
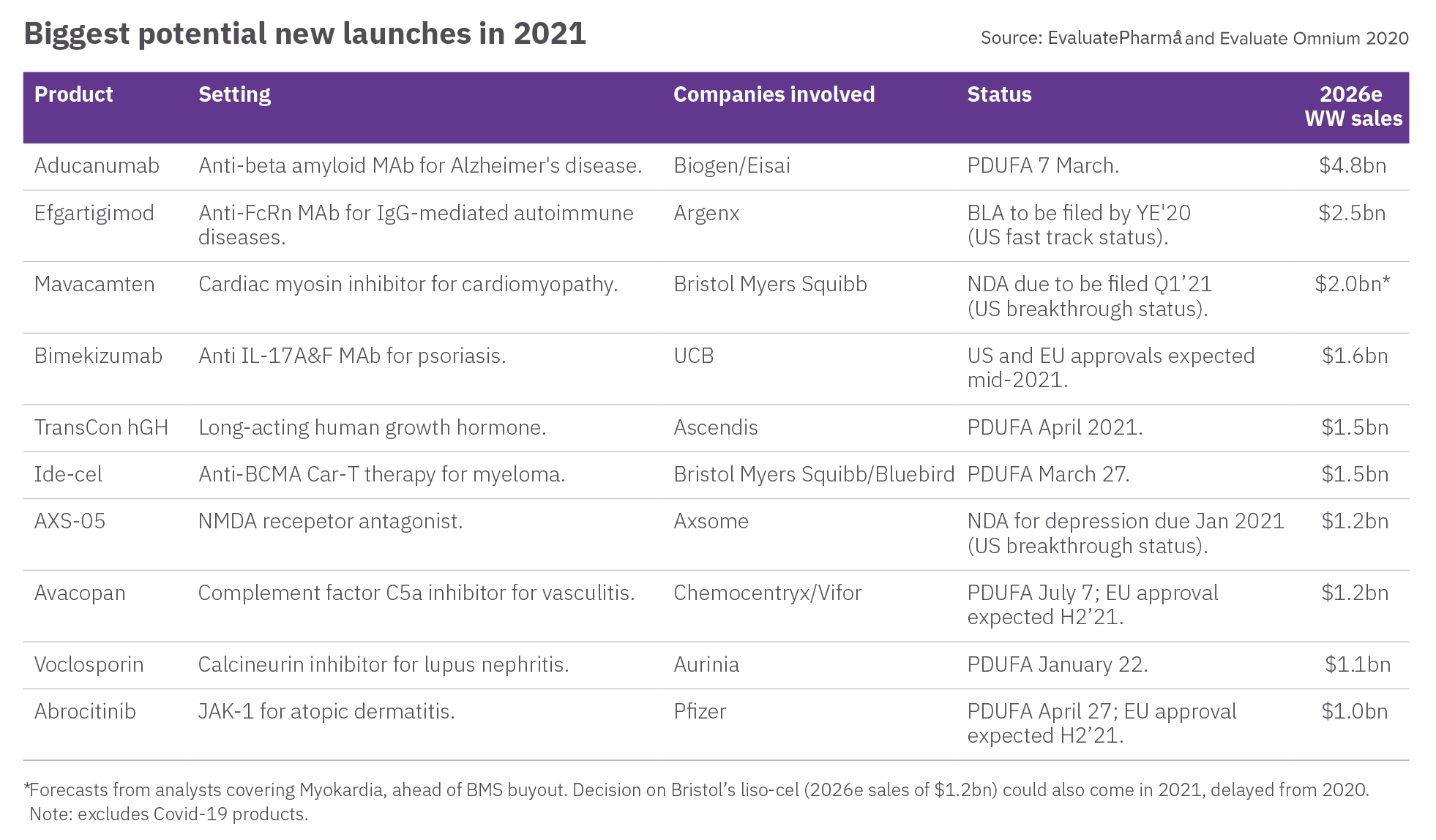
根据 Evaluate Pharma 的预测报告:
“2021年监管机构可能会批准至少10款‘重头药’,其中最值得关注的将是百健公司(Biogen)备受争议的阿尔茨海默症在研新药——阿杜卡玛单抗(Aducanumab)。
尽管市场急需一款对阿尔茨海默症有效的药物,但在由FDA组织的外部专家评审会上,专家们几乎一致投票反对该抗体药物。FDA通常会支持专家委员会的意见;但目前FDA的支持性文件和该裁定引人注目的程度,让最终结果难以预估。无论何种裁定,这次审批都将是生物制药公司2021年最大的事件之一。”
2.“T细胞银行”业务将迎来巨大机会
MilliporeSigma生命科学工艺解决方案主管Andrew Bulpin认为:
“CAR-T细胞疗法为治疗和治愈某些类型的癌症创造了巨大的机会。但生产它们仍面临许多挑战。最大的挑战之一是原材料的质量,因为原材料是从癌症患者身上获得的。当患者接受CAR-T细胞治疗的时候,可能已经病入膏肓,并且已经经历了一系列的治疗,因此获得的T细胞质量不高,或者很难得到合适数量的T细胞。”
“展望未来,我看到了T细胞收集和储存领域的巨大机会。一旦有人被诊断出患有某种癌症,治疗方法第一步就是捐献T细胞冷冻起来。之后,如果传统疗法不起作用,他们可以拥有高质量的T细胞来进行CAR-T细胞
疗法。”
就CAR-T疗法而言,国内进展目前也很快。就在几天前,1月12日,据CDE官网,国内首款CAR-T疗法—复星凯特CAR-T疗法产品的上市申请已经进入行政审批阶段,距离上市不远。CAR-T疗法市场一旦打开,“T细胞银行”的巨大机会对中国医药市场同样适用。
3. 继续青睐利基药物
全力研制重磅原研药,如同淘金者想要找一颗珍贵的大粒金子,不仅需要好技术、好眼力、好耐性,还要有一点“好运气”。在这种情况下,缝隙中的市场,即利基市场,成为最吸引眼球的选择。
辉瑞CentreOne管线开发和创新领导人Nicole Strauss认为:
“利基产品的适应症正在极大地影响新药的开发方式。CDMO与合作伙伴的合作方式以及药物生产的规模将不断演变。越来越多的CDMO将以较小的制造规模来生产,这将需要新的工作方式。”
生产能力
1. 中东和亚洲疫苗产能将扩大
2. 更多的制造业投资将在本地
3. 制造趋向小规模
4. 人才之战将继续
1. 中东和亚洲疫苗产能将扩大
MilliporeSigma生命科学工艺解决方案主管Andrew Bulpin表示:
“从历史上来看,疫苗是由少数公司生产的。但是考虑到COVID-19大流行,个别国家希望有一定程度的疫苗自主控制权。还有一些现金充裕、但产业多样性有限的国家,比如以石油为基础的经济体,它们则可能寄希望于投资新市场。这2点会导致亚洲和中东国家疫苗生产能力的扩大。”
市场动态也显示了这一点,阿联酋正在加紧投资制药业,并将其设立为下一个经济繁荣目标。
生命科学材料领先的温控物流解决方案供应商Cryoport Systems首席执行官Mark Sawicki认为:
“全球COVID-19疫苗和治疗所需的生物制剂和疫苗生产能力将占总可用能力的很大比例。2020年对制造能力的需求增长将持续到2021年,许多公司都在建设自己的内部制造能力以满足需求。”
2. 更多的制造业投资将在本地
瑞典新兴小分子CDMO行业龙头Recipharm表示:
“美国和印度等许多国家的政府现在都鼓励本国制药行业将供应链本地化,或者至少使供应链多样化,以防止未来经济再次停摆时供应链中断。2021年,我们很可能会看到全球制造商重新考虑他们的供应链。”
3. 制造趋向小规模
“细胞和基因治疗等颠覆性技术,将倒逼制药行业快速部署设施,行业将越来越多地使用更小规模的、模块化的、可移动的工厂。这将有助于加快产品上市速度,进一步扩大全球制造足迹,并增加对实时供应链管理和计划的需求。”
—Zenith Technologies首席执行官Joe Haugh
Zenith Technologies是一家总部位于爱尔兰的生命科学制造技术服务公司,专注于数字技术,以管理、控制和优化药品和医疗设备生产,从而提高运营效率和法规遵从性。
4. 人才之战将继续
“制药行业对产能的空前需求已经影响了劳动力。人才大战正在进行。预计COVID-19相关的新型生物制剂和疫苗将陆续获得批准,这些公司也意识到,如果没有合适的人才,无法应对即将到来的加速生产。这促使生物公司建立多样化且可持续发展的团队。”
—路博润生命科学CDMO总经理Barbara Morgan
供应链
1. 疫苗的冷链会回归传统温控
2. HPAPI(高效原料药)市场容量将达
330亿美元
3. 新的API玩家入局;新型原材料抢手
1. COVID-19颠覆了疫苗的冷藏温度,但市场会回归传统温控
COVID-19疫苗对疫苗供应链的一大颠覆是:出现了许多需要深度冷冻的疫苗,即需要零下几十摄氏度保存的疫苗。
但领先的温控包装服务商Pelican BioThermal认为这种情况不会长久存在,冷链需求会趋向于回归传统。
“仅就冷链来说,市场还是会更青睐温度为2-8摄氏度的冷藏疫苗。深度冷冻疫苗的制药公司需要寻求如何在冷藏温度下保持疫苗的效力。如果这种情况发生,行业大概率会开发出新的技术,将药品目前的储存和分发温度从零下80摄氏度提高到更容易分发的范围,比如零下50摄氏度或零下20摄氏度,甚至是2-8摄氏度的冷
藏温度。”
—Pelican BioThermal总裁Dave Williams
2. HPAPI(高效原料药)市场容量将增长
高效原料药(high-potency active pharmaceutical ingredient)逐渐成为原料药厂商收入的重大来源和生产的重中之重。
“到2025年,单是HPAPI市场就将从2016年的160亿美元增长到330亿美元。这些成分帮助创造更有效、更以病人为中心的治疗方法,帮助药品以更少的剂量达到相同的效果。”
“未来,我们可以期待更多的合同服务提供商扩大他们的无菌和HPAPI生产能力,以满足客户对这两方面的更高需求。”
—ChargePoint首席商务官Tony O'Sullivan
ChargePoint为制药、化工、食品等行业提供密封阀门以及综合材料处理设备。
3. 新的API玩家入局;新型原材料抢手
“细胞和基因治疗行业将继续迅速壮大,随着项目纷纷进入后期临床阶段,对原材料的竞争将加剧。疫情让企业意识到供应链的战略意义。企业将考虑如何实施二次采购计划,以及保持大量库存,以最小化缺货风险。这可能导致在载体和API供应商领域出现几家新的竞争对手。”
—Rubius Therapeutics生产副总裁Bryan Gillis
“疫苗的工作流程(例如mRNA和重组蛋白亚基的生产)在制造和配制步骤中需要用到新的原料,同时还需要在规模、文件和杂质表征方面进行逐步改进。另外,我们不要忘记,用于疫苗生产的原材料投入和一次性成分往往与单克隆抗体共享,不仅对操作要求很高,并且对时间敏感。”
“也就是说,高涨的疫苗生产和创新疗法的生产,都需要这些新原料。行业需要创新的解决方案,以同时满足这2个领域。”
—艾万拓(Avantor)生物制药生产执行
副总裁Ger Brophy
制造技术
1. 设备将更加集成
2. COVID将引发许多细节但关键的创新
3. FDA新规敦促制药公司建立更强大的
QC文化
1. 设备将更加集成
“2021年,我们将继续关注设备的运营效率。对于药片压缩设备来说,这意味着额外的转台,以最大程度地提高产量并简化转换过程—或者实现在线药片测试系统,允许一个操作员监控多台机器。压片机控制系统将越来越多地集成到中央工厂系统中,以方便域登录、中央产品配方管理以及中央批次数据存储。”
—高思(KORSCH)美国总裁Fredred Murray
2. COVID将引发许多细节但关键的创新
2021年将迎来人类历史上最广泛最大规模的一次疫苗冷链接种工作,期间将不可避免地遇到各种各样的障碍。
“举一个细节的例子,对于必须在超低温下储存的疫苗来说,其中一个“微观因素”就是粘接剂,比如用胶水粘合在一起的许多二次包装折叠纸箱,粘合剂无法承受超低温冻结,胶水结晶膨胀,纸箱接缝就会破裂。这导致像纸板这样简单的包装环节,都会变得举足轻重。也直接引发了无胶纸箱的创新设计。”
—Keystone折叠盒公司
营销和业务发展总监Ward Smith
3. FDA新规敦促制药公司建立更强大的QC文化
“FDA已经宣布了质量管理成熟度(QMM)试点计划。该试点的目的是将第三方对制造商质量管理体系的评估纳入参考,进一步完善FDA评级体系。就像FDA公告中说的,对于拥有成熟质量管理体系的制造商,FDA可以采取更灵活的监管方式。最终目的是,即使没有广泛监管的情况下,也可以保证制药界高质量的药品生产。
除此之外,COVID-19让公司转向创新模式,开发新的疗法、测试方法和疫苗来对抗疫情。并且速度要快。
新规和疫情,最终结果是一样的:加速质控和制造流程进一步数字化集成在一起,只有这样,制造商才能够在保持最高质量水平的同时快速交付产品。”
—MasterControl实验室总裁Matt Lowe
MasterControl QMS是一家全球化的质量管理系统解决方案,有医药、医疗、生物制品等合规行业的客户上千家,亚洲客户近两百家,每年有20%以上的增长,是全球具有客户稳定性和增长性最高的质量管理系统QMS之一。
药物开发
1. 个性化药物研发热度高涨
2. 预充注射剂市场保持10.4%增长率
3. 研发将聚焦“免疫”
4. 传染病投资将增加
5. COVID-19将使临床试验持续紧张
1. 个性化药物研发将继续
“业界的普遍预测是,对研发的投入重点将集中在早期疾病检测方法的开发,个性化医疗将迎来发展,为患者进行定制的药物开发,以及基于对不同疾病的机制研究,开发更精确、更有针对性的药物疗法。”
—ACG Engineering销售副总裁John Carey
2. 预充注射剂市场保持10.4%增长率
“市场对创新产品的需求上升,许多产品将通过预充式注射器交付。过去十年,通过自我给药治疗慢性疾病或进行家庭保健,已成为广泛趋势,无菌注射剂在抗血栓药、疫苗、血液刺激剂、干扰素、类风湿性关节炎等领域得到广泛应用。预计到2026年,全球预充式注射器市场规模将达到95.3亿美元,复合年增长率10.4%。”
—Nicole Strauss,辉瑞CentreOne管线开发与创新负责人
3. 研发将聚焦“免疫”
“疫情延缓了肿瘤学等疫苗以外的其他领域的研发,目前正在慢慢回归正轨。这带来了很多不确定性,尽管就投资而言,肿瘤仍就是领先的研发领域,但我们开始看到对免疫的真正关注。癌症很难治疗的原因之一在于—它来自于你自己的身体。这使得在不杀死其他细胞的情况下很难瞄准目标。”
—路博润生命科学健康部CDMO总经理Barbara Morgan
4. 传染病投资将增加
“迄今为止,肿瘤适应症一直是制药和生物技术领域最具吸引力的资本投资目标。虽然许多新的治疗方法,从CRISPR到mRNA和细胞治疗已经获得了势头,但它们主要针对各种液体和固体肿瘤。在过去,尽管传染性疾病对全球总体健康有很大的影响,但获得的投资相对较少。吉利德的瑞德西韦是为埃博拉病毒开发的,但在COVID - 19取得了成功。这可能会激励到制药商和投资者将更多资源分配给目前价值较低但影响力大的传染病适应症,但不是冠状病毒。”
—RI Bio入驻企业家Jay Round
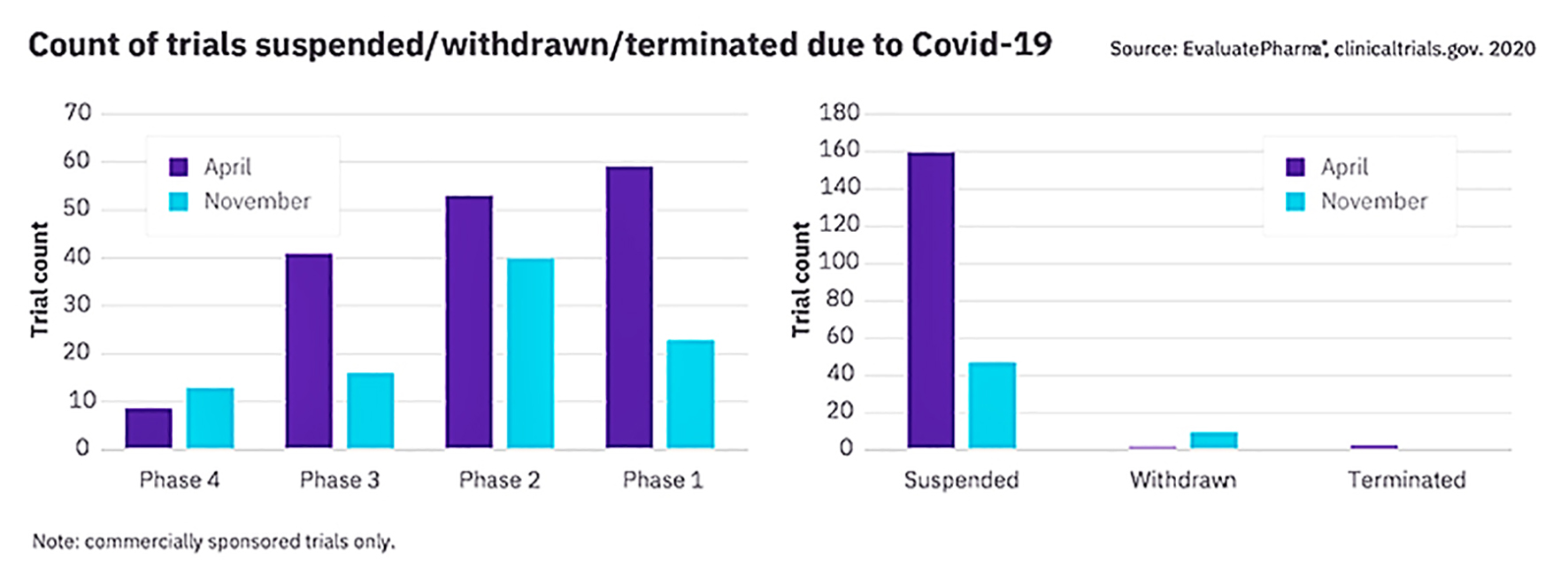
5. COVID-19将使临床试验紧张
“由于新冠肺炎疫情,许多临床试验将继续面临登记患者不足的难题。这将对仍在运行的试验数量产生负面影响,并限制2021年新项目的数量。”
—Cryoport Systems首席执行官Mark Sawicki
法规变更
1. 审查解封,保持高效率
2. 监管机构将利用起数字工具
3. EMA附件1(无菌制造)将有重大更改
1. 疫情解封了审查效率,这种高效或将保持住
“疫情的特殊情况,迫使监管不得不省略很多流程,审查速度一下子解除 ‘封印’ 了。”
“COVID - 19的一个大问题是,疫情会一波接一波地爆发,在不同的时间点,不同设施的生产能力会下降。因此,许多公司不得不申请批准将生产转移到另一个地点。这一过程可能非常复杂,但在疫情期间必须非常迅速地完成。因此,行业会重新审视这些快捷流程:尽管没有走完全部的审查流程,但如果一切顺利,未出问题,为什么不沿用这样的高速审查呢?”
—Informa Pharma Intelligence分析师Bowman Cox
2. 监管机构将利用数字工具
“监管机构将继续利用新的远程技术,从记录、审查到产品抽样和质量测试。在即将上任的拜登政府的领导下,监管机构之间的国际合作也将继续改善。这意味着,您应该为一个不可避免的事实做好准备:与你合作的任何检查员,无论他们代表的是哪个监管机构,都将与世界各地的同行分享他们收集的信息!”
—Stericycle危机解决方案副总裁Chris Harvey
3. EMA附件1(无菌制造)将有重大更改
“我们将看到一个完全不同的EMA附录1(无菌产品的生产文件)。关于该草案的争议充分反映了当今全球无菌产品生产的多样化。虽然欧洲药品管理局(EMA)可能认为该附录没有争议,但主要生产商和相关机构提出了很多疑问,包括:
1. 该文档是基于20世纪70年代后期使用的技术,这限制了它在当今更加自动化的处理环境中的实用性;
2. 过分强调抽样和测试来确认工艺/产品的适用性,这与广泛使用的工艺验证是相悖的;
3. 草案没有认可强大的无菌处理技术的价值,基本上把这些技术的性能等同于有人值班的洁净室;
4. 继续将环境监测、无菌测试和工艺模拟的可靠性奉为无菌性的决定性证据;
5. 编写不够清楚,不能被全球许多国家/地区众多生产商所理解。
关于第二稿提出的广泛争议表明,无菌制造行业在观点上仍存在实质性差异。今年EMA附件1将要被进一步修改。”
—制药和生物技术服务商Agalloco&Associates
总裁James Agalloco
市场走向
1. 修美乐暂保王冠,K药将接替为王
2. 并购将反弹
3. 生物制药革命将扎根
1. 修美乐暂保王冠,K药接替为王
“肿瘤学将继续成为2021年该行业营收增长的主要驱动力。十大最大的新销售来源中有六种是各种癌症的治疗方法,其中三种是PD(L1)抗体。默沙东的K药可瑞达(Keytruda)就是其中的王者,K药预计将在2023年成为世界上销量最大的药物,取代艾伯维(Abbvie)的修美乐的王冠。”
—Evaluate Pharma的Vantage 2021报告。
2. 并购将反弹
“2020年,制药行业的并购交易减少了,比2019年减少了约40%。现在,高管们看到了隧道尽头的曙光,疫苗正在被广泛分发,新规的刺激措施即将来临。制药公司还瞄准了更困难的治疗领域,例如中枢神经系统疾病和阿尔茨海默氏病,因此它们必须依靠外部创新。
2019年,制药业并购交易达到3780亿美元的历史新高,但在过去十年中,平均每年约为2000亿美元。我们预计,到2021年,并购至少会反弹回到2000亿美元的水平。”
—安永美国科学与健康行业市场负责人Arda Ural
3. 生物制药革命将扎根
生物分子,生物系统,生物机器和生物计算,共同构成了“生物革命”。COVID-19疫苗的开发,只是所谓的“生物革命”潜力的一个例子。
在MGI(麦肯锡全球研究院)2020年5月发布的报告中指出:生物学相关的创新,在未来10~20年内可减轻全球疾病总负担的1%~3%,大约相当于消除肺癌、乳腺癌和前列腺癌的负担总和。如果能够充分发挥生物科学潜力,则可以使用当今可行的科学技术来解决全球疾病负担的45%。
“例如,基因编辑技术可以遏制疟疾,疟疾每年杀死超过25万人。细胞疗法可以修复甚至替代受损的细胞和组织。新型疫苗可以应用于包括癌症和心脏病在内的非传染性疾病。
生物革命的潜力不止是在医药领域。根据MGI的说法,随着时间推移,占全球经济产出60%的产品将能够通过生物学手段来生产。
例如:尼龙已可以由转基因酵母代替石油化工产品来制造;“皮革”可以由蘑菇的根制成;“水泥”可以由细菌生产;进行基因改造以培育耐热/抗旱作物或解决诸如维生素A缺乏症的状况;通过基因工程改造的微生物来制造生物燃料;还有人工蜘蛛丝、自修复织物.....
根据目前的技术能力,这些应用都是可行的,可能在未来10年创造数万亿美元的经济影响。”
— 麦肯锡全球执行合伙人Kevin Sneader;
麦肯锡全球医疗保健负责人、高级合伙人Shubham Singhal
来源:荣格-《国际医药商情》
原创声明:
本站所有原创内容未经允许,禁止任何网站、微信公众号等平台等机构转载、摘抄,否则荣格工业传媒保留追责权利。任何此前未经允许,已经转载本站原创文章的平台,请立即删除相关文章。