荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
吸入给药的一个定性特征是患者接受的剂量存在可变性,它可能是由不同原因引起的,例如患者的生理结构,或是使用过程中所采用的技术等。上述可变性能直接影响到临床效果,因此将其降低到最低限度是业界内一个重要的追求目标。是以,尽可能求实的对待患者使用吸入剂的方法,以及采用尽可能成熟的配方是提高治疗方案有效性的重要策略。
压力型定量吸入气雾剂 (MDI) 是哮喘、慢性阻塞性肺疾病和其他呼吸系统疾病治疗的第一线常用药。在日常使用中,随着患者在家庭与工作/学习场所之间往返或参加户外活动,这类MDI会自然而然的经历不同的温度环境变化。因此在面对温度骤变的情况下,确保吸入器保持充分装填的状态,即“随时可用”状态,才能保证每次使用时都药量充足,继而达到有效的临床使用剂量。
本文对因温度变化而造成的MDI‘充填量损失’机理进行了探讨。对市面上三种采用不同推进剂配方的MDI在不同温度循环下的表现进行了实验研究,也就上述变化对临床实践、患者体验以及产品设计的效果意义进行了检验。
MDI的初始化充填和充填量损失
MDI配方药剂的主要形式是溶液或悬浮液产品,采用蒸发推进剂散发喷雾,形成重复剂量给药。自50年代首次推出按压-吸入式设计以来,大部分商业吸入器的设计并没有发生太大的变化,一直依赖于相对简单的操作原理。一旦按压,吸入器的剂量腔就对金属罐里所承载的剩余药剂闭合而对大气开放,从而使推进剂配方药剂膨胀并通过开合口后雾化。雾化后的药剂含有大量的细颗粒成分 (FPF) (通常其空气动力学颗粒粒径不超过5µm)。
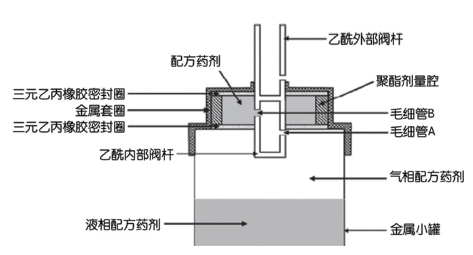
图1:Bespak BK 357 MDI毛细微保持阀原理示意图 (毛细管A&B的直径 = 0.6mm)。
MDI的一个关键部分是如图1所示的毛细微保持阀,它对开合后药剂量进行预先计量,为患者后续使用做好准备。在药物充填过程中,由于气门阀杆孔端口的压差,装在金属小罐里的液态药剂通会过两根毛细管被抽吸到剂量腔内。这种设计背后的科学原理十分可靠,不过在特定的环境下,反引力可能会超过毛细管保留力 (Rayleigh Taylor理论),使配方药剂从剂量腔回流到金属小罐内 (Fradley and Hodson, 2008)。除非MDI在使用前预先充填好,不然上述情形就有可能造成不稳定剂量。
吸入器在温度变化下也有可能因为其内部产生的临时温度梯度而使药剂充填量发生变化。这是因为吸入器的各个部分采用不同材料制造,它们的升温和降温速度就会各不相同。比如,具有高导热性能的金属小罐与不导热聚合物计量阀的组合会导致与金属小罐相连的剂量腔内产生较高的蒸汽压,并引起回流 (Lewis et al., 2011)。也有证据表明,所采用推进剂的种类也对该效应有一定的影响,研究表明,HFA 134a配方药剂要比那些包含乙醇类配方的药剂更容易损失充填量 (Church et al., 2011)。在下面展示的研究中,我们对在温度循环下HFA 134a配方药剂和含乙醇类配方药剂的充填量损失进行了对比研究,从而对上述的变化特性进行了阐述。
案例分析:
受控及现实环境条件下温度循环的影响评估
我们对三种固定剂量的商用MDI:Foster® (Chiesi), flutiform® (Mundipharma)和Seretide® (GlaxoSmithKline) 分别进行了在温度循环下表现的实验研究 (Lewis et al 2016)。每个产品都包含吸入型皮质类固醇 (ICS)和长效β2-受体激动剂 (LABA),并且采用毛细微保持阀进行药剂剂量的计量。但每种产品又在所采用的计量阀,配方药剂的形态(溶液或悬浮液),以及推进剂/赋形剂配方等方面都各不相同(见表1)。每种处于有效期内的MDI产品都取了5个单位量参加测试。
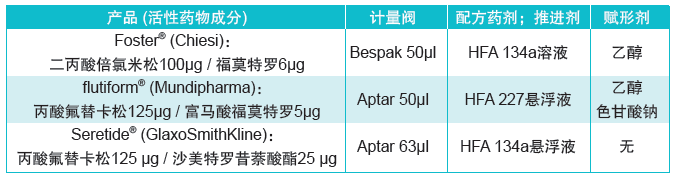
表1:用于剂量保留测试的三种商用MDI的容器密封及配方特性。
本次实验的前两种是模拟现实生活中的温度循环,以评估温度变化对喷雾给药量的影响;而第三种模拟是将MDI药剂置于更严格控制的条件下(见表2)。每种模拟实验都使MDI药剂在两种不同温度环境之间往返循环5次,所有MDI药剂在不使用的情况下都保持阀门向上的储存状态。
为确定基准喷雾药量(SSWs),每种药剂产品都根据患者使用手册 (PILs)中的指南和标准药典测试方法来使用剂量单位取样装置 (DUSA) 进行取样,以确保测试中MDI药剂剂量的一致性。每组模拟实验中,药剂样品都被加以五次方法类似的温度循环,每次循环后对未充填喷雾药量(USW)进行了测量。USW对SSW的比值百分数即计为剂量保留值。此外,ICS和LABA的给药剂量以及后续药剂余量也在模拟实验3中通过每次温度循环后的5个连续的剂量进行了测试(对Seretide®的LABA测量除外)。
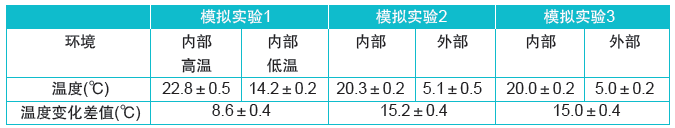
表2:药剂产品环境模拟实验的温度条件 (n=5)。
表3列出了药剂产品被置于温度波动下剂量保留值的变化。对Foster®产品而言,15℃以下的温度变化对USW/SSW值没有影响,该值在三组模拟实验中始终保持不变。相反地,flutiform®产品的表现仅在模拟实验1中维持不变。当温度差值增加到15℃时,剂量保留值会有下跌并同时低于现实和受控环境的范围。而Seretide®的USW/SSW值在吸入器置于模拟实验1的条件下跌至100%以下,并在温度变化增加至15℃时进一步有下跌到现实和受控范围以下(模拟实验2和3)。
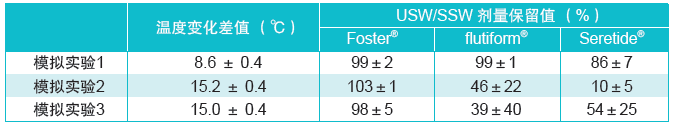
表3:不同温度循环模拟实验下的剂量保留值% (USW/SSW) (n=5)。
相对于另外两个产品,Foster®的性能更加可靠,这可能得益于其相对较高的乙醇含量(12%w/w),这一发现与之前的研究结论也相一致(Church et al., 2011)。同时也就能合理解释乙醇含量1.3% w/w的flutiform®相对于无乙醇配方的Seretide® 有略好的表现。由此可以得出结论,MDI配方药剂中加入乙醇配方赋形剂有助于改善剂量给药相对于温度变化的稳定性。
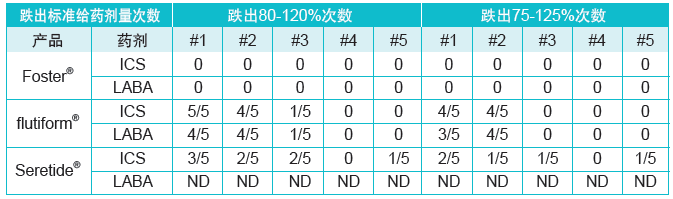
表4:受控温度循环条件下测量ICS和LABA剂量跌出标签注明标准给药剂量的次数 (模拟实验3),ND=未确定。
图2显示了配方药剂中活性成分在严格控制温度循环影响下的给药剂量。Foster®再次显示出最稳定的性能,在所有模拟实验情况下的ICS剂量给药量都在标签注明的80-120%范围内。相反地,flutiform®和Seretide®的未充填ICS给药剂量则大大低于标签注明量。LABA的测试数据也遵循同样的趋势。总体而言,在模拟实验3的五次温度循环测试后, flutiform®和Seretide®的吸入剂配方药的连续给药分别有10次和8次剂量给药后跌出80-120%的标签注明量范围,而flutiform®和Seretide® 的给药剂量跌出75-125%的标签注明量的次数则分别达到了8次和5次( 见表4)。
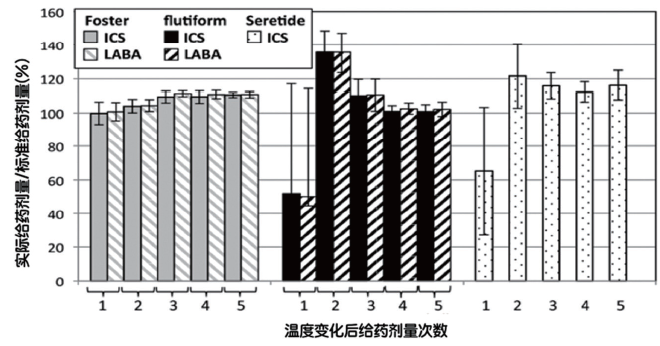
图2:模拟实验3后ICS和LABA给药剂量占标准给药剂量 (按药剂标签规定) 的百分比% (n = 5)。
一个有趣的现象是,当flutiform®和Seretide®继温度循环后喷出的第一下低于标签注明的剂量后,之后紧接着的一次喷给药量的ICS含量反而大大高于标签注明剂量。这一现象表明,药剂充填量损失是与API在剂量腔中的沉积有关的,由于剂量腔内存在沉积的药物, 所以当重新填满后,积淀的药剂就会累积到下一喷中。
flutiform® 和Seretide® 在温度变化下跌出标签注明剂量的次数也很值得关注,这是因为食品及药物管理局的导则建议,为保证药剂的剂量一致性处于可接受的范围之内,剂量次数可以跌出80-120%的标签注明剂量不能超过十分之一。很明显,这两种产品必须在使用前进行充填从而达到上述导则的要求,这在它们的患者使用手册上也有相关的注明:说明中建议患者在正式使用其吸入剂进行治疗前先试喷四次 (flutiform®) 或两次 (Seretide®) 初始化充填量(标签注明为120喷剂量)。此外,flutiform® 的患者使用手册推荐不仅在首次使用前进行初始化充填,如果吸入器三天或三天以上未使用,或暴露在冰冻或冷藏的温度条件下,也需要重新充填。Seretide®则对寒冷温度条件并没有明确的建议。不过,这两种产品的设计用法是每天常规使用两次,而非用于急救,因此暴露在温度波动下及相应充填量损失的情况不太可能产生严重的问题。
展望未来
为患者日常使用设计出能经受严峻考验、保持性能稳定的可靠吸入药剂产品是业界的一个重要目标。因为患者会不可避免的将MDI置于一定的温度波动下,尤其是在用于急性症状缓解的情况下。本文实验结果显示,这类温度波动有可能会造成MDI药剂从计量腔回流,充填量损失和给药剂量不够精确等现象。当然,这个问题可以通过培训患者始终在使用前对吸入器进行充填加以解决。不过,本文实验结果还提出了一个更基础的方法,那就是妥善设计药剂配方组成,尤其是通过选择不同赋形剂的方法。上述发现为开发性能更稳定、使用更可靠的MDI开辟了一条新的道路,从而对药物的临床有效性提供了更多的保证。
参考文献:
Church, T.K., Hargrave, G.K., Johnson, R., Lewis, D.A., O'Shea, H., Versteeg, H.K., (2011). Visualising dose retention: fluctuation on a pMDI capillary retention model. Respir. Drug Deliv. 317 – 320.
Fradley, G., Hodson, D., (2008). Optimisation of fluid flow in pMDI valves. Respir. Drug Deliv. 2008, R.N. Dalby, P.R. Byron, J. Peart, J.D. Suman, S.J. Farr, and P.M. Young (eds), Davies Healthcare International Publishing, River Grove, IL, Vol 2, pp. 329-332.
Hess, D.R., Myers, T.R., Rau, J.L., (2007). A guide to aerosol delivery devices for respiratory therapeutics. American Association for Respiratory Care. http://hallowell.com/media/aerosol_delivery_guide.pdf Last accessed 14th July 2016.
Lewis, D., 2007. Metered dose inhalers: Acutators Old and New. Expert Opinion on Drug Delivery 4 (3), 235-245.
Lewis, D.A., O'Shea, H., Church, T.K., (2011). Prediciting HFA-MDI dose retention properties: engineering the marriage between canisters, valves and formulations. Respir. Drug Deliv. Europe, 89 – 99.
Lewis, D., O'Shea, H., Mason, F., Church, T.K.. 2016. Exploring the impact of formulation and temperature shock on metered dose inhaler priming. http://www.tandfonline.com/doi/full/10.1080/02786826.2016.1240354. Last accessed 12th January 2017.
Newman, S.P., 2005. Principles of metered-dose inhaler design. Respiratory Care 50, 1177 – 1190.
Newman, S., Peart, J., (2009). Pressurized metered dose inhalers. In Respiratory Drug Delivery: Essential Theory and Practice, Newman, S. (ed), Davies Healthcare International Publishing, River Grove, IL, Chapter 6.
Tamura, G., 2015. Comparison of the aerosol velocity of Respimat® soft mist inhaler and seven pressurized metered dose inhalers. Allergology International 64 (4), 390-392.
Thiel, C.G., (1996). From Susie's question to CFC free: An inventors perspective of forty years of MDI development and regulation. Respir. Drug Deliv. V, R.N. Dalby, P.R. Byron, and S.J. Farr (eds), Interpharm Press, Buffalo Grove, IL, pp. 115-124.