荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
生物仿制药如同凤凰一般,在几款生物制剂面临排他损失之际,从制药市场的灰烬中发展成如今新型行业。预计到2018年,全球这一市场将达到20亿美元。
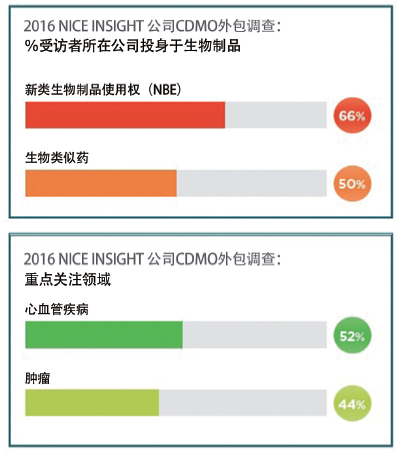
尽管目前在美国只有四家代理获批,在欧洲的数量已超过20家。这一发展正在加速,据估计,目前有30家公司曾积极投身此项事业,大约有56款生物仿制产品正处于研发管线中。事实上,根据Nice Insight公司在2016年CMDO外包调查中,50%的被访者目前从事推动生物仿制药发展的工作之中。卫生医疗系统在处理药物成本上升和使用准入门槛上对于生物仿制药提供重大的机遇。此外,从商业角度而言,生物仿制药在中长期也可被视作为一个诱人的机会。预计到2020年,约有价值1100亿美元的生物制剂会面临专利到期的窘境,而这占据了制药企业大约三分之一的生产管线。如果企业能够结合另外两个重要的发展契机,包括控制医疗成本方面日益增加的压力以及生物仿制药监管透明度的大力提升——机遇显而易见。
研发和生产生物仿制药品给未来带来了一个引人注目的和有价值的命题。在专利排他性失效之后,病人被允许有了更多的选择权,竞争将更为激烈,整体医疗成本也将降低。生物仿制药可以帮助医疗系统在降低成本的同时,提供安全有效的替代生物药物的品牌。
Sandoz公司北美区域生物制药部门副总裁Gregory Oakes表示:“患者和供应商可以相信,如果一款生物仿制药被FDA 授权批准,那一定是安全的,并且其功效和质量与原研产品是同等的。”Oakes先生继续提到,Sandoz在2015年9月推出了美国第一款生物仿制药Zarxio,这是针对嗜中性白血球减少症的大剂型药物的仿制药。“Sandoz领先推出研发管线中的这一产品,我们也很满意Zarxio迄今为止在美国的表现。”Oakes先生补充说,“我们的市场份额是符合预期,且超过基准。”在欧洲,Zarxio( 欧洲区域商品名) 拥有超过30% 的市场份额。它是第一款推出的生物仿制药并超过其参考产品( 安进公司的Neupogen) 和市场领导者Chugai 公司的Granocyte。
生物制药的负担
生物仿制制药公司需要大量投资和长期的承诺将他们推向市场,包括成本的开发、管理、报销和知识产权诉讼的挑战。此外,在美国批准的监管途径是相对较新的,最新批准的BPCI 法案(Biologics Price Competition and Innovation Act),也是2010年批准的可支付医疗法案内容的一部分。
人们普遍认为生物制剂的监管阻力是一个减缓其进入市场的因素。尽管FDA不会公开评论生物仿制药品法规,在美国所有获批的生物仿制产品必须符合FDA 严格的标准证明。病人也可以预期相同级别的质量、安全性和有效性的生物仿制产品作为参考。
欧洲目前在生物仿制药市场上占据主导地位,这不足为奇,因为欧洲的监管部门批准自2006年开始授权使用生物仿制药,如今在欧盟已有近20个产品。亚太是第二大区域市场, 其次是其他新兴地区包括南美洲、以及生物仿制产品已经注册在澳大利亚、加拿大、印度、日本和韩国。许多生物仿制开发人员有针对性的瞄向亚洲和其他新兴市场,因为其审批过程往往是简单的。许多业内人士认为, 这些产品都不是真的生物仿制药,因为批准授予之际并未要求任何对比原研药的演示,而这在欧盟和美国则是获得监管批准的一项重要关键的步骤。这一点应当值得注意,许多国家都在发展的过程中针对特定的生物仿制药,其审批路径或指导方针尚有疑问,包括澳大利亚、马来西亚、巴西、墨西哥、委内瑞拉、哥伦比亚、印度、俄罗斯和中国。
生物仿制药品的开发和生产成本实际上相当庞大。该生物制药只有在预计将获得适当的美国市场份额时,才有可能实现降低利润率。“如果监管条例以及经济条件都不利于制药企业将生物仿制药推向市场,那就不会有一个健壮的生物仿制药行业。”Ciny曹女士这样表示。她作为Sandoz公司生物制药管理事业部的总经理,发表了如下看法:“这意味着对于政府决策人士而言,了解某些政策决定的后果对于美国生物仿制药市场的发展是至关重要的,这将帮助创建理想的市场动态,并助力生物仿制药行业茁壮成长。”“拥有正确的监管框架和政策对仿生物药品的持续增长至关重要。”曹女士强调,“Sandoz正在积极参与政策制定, 以确保病人得以长期使用这些药物。与卫生部门合作和分享新的科学发展规划是很重要的。”
健康系统的成本节约
预计到2020年,生物仿制药在美国和欧洲,在健康系统方面所节约的成本预计将达到1100亿美元。Oakes表示:“如此成本节约主要驱动因素来源于企业的竞争。”2013年,生物制剂约占美国药品总支出的28%(总计支出约为920亿美元),相比2012年增长了近10个百分点。RAND公司预测从2014年到2024年,生物仿制药将直接减少442亿美元的生物制剂的支出。粗略估计该金额将占同期生物制剂开支的4%,可能从130亿美金至660亿美金。Generic制药协会则估计在未来十年里生物仿制药节省的净额将从440亿美元增至2500亿美元。
因此,针对生物仿制药日益增长的需求以及认知正在驱动这一市场。生物仿制药被认为现今在治疗慢性疾病方面具有广阔的前景,例如癌症和心血管疾病。2016年Nice Insight公司一份CRO外包报告中指出,52%的受访者认为心血管疾病是重点的治疗领域,44%的受访者则表示肿瘤将是他们的目标重点。因此,明智的市场人正致力投资生物仿制药市场以便创造更多的机遇。
参考资料
1. Biosimilars: Preparing for the Revolution, Ebix.com, Aug. 19, 2016
2. The 2016 Nice Insight Contract Development&Manufacturing Survey
3. Rise of biosimilars in the US, PharmaLive, June 8, 2016
4. Information for Healthcare Professionals (Biosimilars), U.S.Food & Drug Administration, May 10, 2016
5. Mulachy, Andrew W., et. al., The Cost Savings Potential of Biosimilar Drugs in the U.S. RAND Corp., 2014
6. Arnoff, Steve, Generic Drugs Continue to Deliver Billions in Savings to the U.S. Healthcare System, GPhA, Oct. 19, 2016