荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。

当前印度企业的增长速度一直快于MNC(跨国公司)制药企业,其中慢性疾病领域以及新产品上市持续推动印度企业的发展。鉴于NLEM(国家重点药物目录)的关注事项,引入许可和收购一直都是重要议题,企业一直专注于进入细分市场领域,例如创新给药系统、综合疗法领域、生物相似药等。一部分处于前端位置的制药企业在次级市场中表现不佳,主要原因有三点,分别是奖励/其他折扣的中断;低利产品、渠道库存等的合理化;急性病治疗领域的增长较缓。此外,一些较小的或是中等规模的企业却维持着较快得增长,显而易见其增长原因是依赖于“纯粹仿制药”的发展。
印度制药企业最值得关注的三大发展机遇或挑战
1:临床试验市场
印度是临床试验市场的领导者之一,因为人口具有基因多样性,并且拥有经验丰富的医生,印度的临床试验市场有潜力获得大量的投资。
2:进入农村市场
印度有70%的人口居住在农村地区,制药企业在这一市场中大有可为。同时,农村地区对仿制药的需求有了显著的增长。众多的制药企业正在对农村地区的分销网络进行投入。
3:合同制造及服务
该市场中的企业已经超过1000家,根据估计合同研究&制造服务行业(CRAMS)2015年达到了80亿美元,远高于2012年的38亿美元,因此具备巨大的投资潜力。
鼓励印度制药企业发展的本土新政策
◆ 2014年9月印度政府出台措施鼓励跨国企业以及国内企业在印度本土生产自己的产品;
◆印度制造的25个核心经济领域中包括制药行业。25个领域允许100% 的FDI(对外直接投资);
◆到2016年2月,投资承诺已经达到2220亿美元;
◆制造企业享有地区税收优惠政策。
摆脱美国“警告信”阴影
有相关数据显示,2015年九家一流企业在美国仿制药的收益为61.91亿美元,相比2014年56.63亿美元增长了9.3%。2016年截至目前已有收益 32.04亿美元,显示该行业的发展势头维持在中等水平。其原因除了竞争加剧;分销渠道整合所导致的基础业务的价格压力对发展产生了影响之外,还存在FDA 法规依从性问题的企业在ANDA(美国简略新药申请)的审批方面呈下滑趋势。但鉴于有众多的在研产品并且复杂分子持续受到重视,因此总体的预期仍然保持乐观。
该领域另一重要风险因素即美国FDA更为严格的监管。印度工厂接到的警告信(WL)的数量在过去几年中已经明显增加(详见表1),其中有大约40%升级为进口预警(IA),对企业的业务造成了严重影响。值得庆幸得是,大型企业解决问题的跟踪记录更为良好;平均的解决问题的周期为大约24个月,50%的在1年之内解。
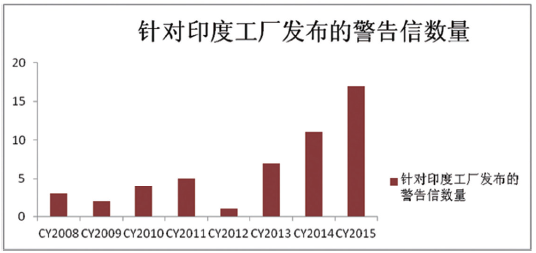
表1:警告信发出的趋势
虽然警告信问题对印度制药企业带来了负面影响,但是通过众多的在研药品对近期业内的发展前景充满信心。不仅仅是因为大部分一流企业一直都有多种提交ANDAs的在研药品,同时伴随着复杂/细分市场的分子所占比例的增加,在研药品的质量随之逐步提升。(文中内容编译自Subhash Gore博士题为“印度制药公司的仿制药全球布局和发展战略”的演讲)
相关链接:
2010年全球知名的医药咨询公司IMS Health发布数据显示印度制药产业已超过100亿美元的产值,并以年增长率15-20%持续快速增长中。当时发展主因是印度国内国民收入的增加,国内保健意识逐渐提升,印度政府的医疗保健预算持续大幅增加等等。
作为世界第三大仿制药生产大国,过去3年印度制药业平均增长速度在14%左右,印度生产了全球20%的仿制药,并使制药业成为印度经济的支柱之一。目前,印度药品出口到200多个国家,疫苗和生物制药产品出口到150个国家。根据Worlds Richest Countries相关数据,2014年印度出口价值117亿美元的药品。10个国家进口的药品占到56.5%(详见表2)
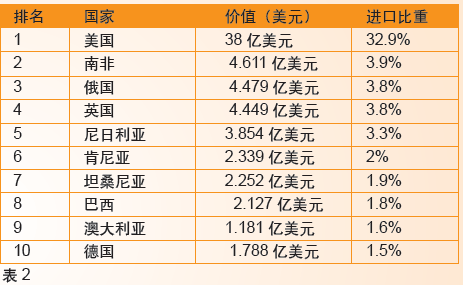
2020年左右,许多专利药将陆续到期,不少专业机构早在几年前就预测,这将会大大刺激印度仿制药的生产,届时印度仿制药预计在全球仿制药市场的份额会从目前的20%增至25%,印度制药业营业额将会从现在的约258亿美元增长到500亿美元。
通过美国FDA认可的印度药厂生产成本比美国低65%,比欧洲低50%。目前印度境内拥有FDA认证的药厂共有119家,可向美国出口约900 种获得FDA批准的药物和制药原料;拥有英国药品管理局认证的药厂也有80多家。